Introducción
Las infecciones fúngicas, en particular las causadas por especies de Candida , plantean desafíos significativos en el ámbito clínico, especialmente en pacientes inmunosuprimidos (1,2). La capacidad de estos hongos para formar biopelículas contribuye a su resistencia en los tratamientos antifúngicos. Las infecciones asociadas con la atención de la salud (IAAS) sobre todo en catéteres vasculares son las más comunes y representan un 5 % de este tipo de infecciones; lo que sugiere retirar el implante o dispositivo para alcanzar tasas de curación mayores al 90 %; y en caso de no retirar el implante, el fracaso oscila hasta un 50 %, lo que provoca infecciones persistentes y un aumento de la morbilidad y la mortalidad (2,3).
Las especies de Candida , como Complejo C. albicans , Complejo Nakaseomyces glabrata , Complejo C. parapsilosis y C. tropicalis , presentan variabilidad en las concentraciones mínimas inhibitorias (CMIs) a los antifúngicos, lo que complica las estrategias de tratamiento (3). Los métodos tradicionales para evaluar la susceptibilidad a los antifúngicos a menudo no tienen en cuenta las características únicas de las biopelículas sésiles, que son menos sensibles a los antifúngicos en comparación con sus contrapartes las biopelículas planctónicas (4,5). Esta resistencia es la responsable de que este tipo de infecciones se perpetúen, reaparezcan y ocasionen daños colaterales en los tejidos circundantes. Estudios han demostrado que las biopelículas de Candida spp., en su forma sésil son resistentes a la anfotericina B desoxicolato, fluconazol, flucitosina, itraconazol y ketoconazol (2,4,6-8).
La utilización del colorante de óxido reducción como resazurina se ha convertido en un método prometedor para cuantificar las biopelículas viables gracias a su capacidad para reflejar la actividad metabólica, lo que proporciona una evaluación más precisa de la sensibilidad a los antimicóticos de las células fúngicas dentro de las biopelículas (3,6,9).
Es por ello por lo que en el presente estudio se plantea valorar la utilidad de la resazurina como indicador colorimétrico en la susceptibilidad a biopelículas sésiles de Candida spp., aisladas de hemocultivos frente a fluconazol, como uno de los principales agentes antifúngicos más utilizados en la práctica clínica.
Materiales y métodos
Investigación de tipo observacional, descriptiva, retrospectiva y transversal.
Muestra
La muestra es de tipo intencional, no probabilística, de 20 aislados del Complejo Candida albicans , 20 aislados de Candida tropicalis , 20 aislados del Complejo Candida parapsilosis , y 20 aislados del Complejo Nakaseomyces glabrata obtenidos a partir de muestras de sangre, las cuales estaban almacenadas y conservadas bajo el método de preservación en agua destilada estéril de Castellani (10). De este total de cepas se utilizaron las que fueron caracterizadas como productoras de biopelículas, determinadas en un estudio publicado con anterioridad a través del método semicuantitativo con tinción de Cristal violeta (11).
El diseño de este estudio no contempló procedimientos experimentales con seres humanos ni animales, ni con muestras biológicas derivadas directamente de estos; se trabajó con cepas fúngicas. Sin embargo, por ser estas cepas provenientes de muestras humanas, los investigadores se comprometen a mantener la confidencialidad de la identidad de los sujetos fuente de estudio, así como la información suministrada y obtenida durante el proceso de investigación cumpliendo con la declaración de Helsinki.
Preparación y viabilidad de los aislamientos: Se tomó una alícuota del medio de preservación y se inoculó en caldo infusión cerebro corazón (CBHI, OXOIDUSA) + extracto de malta (HiMedia-India), y fue incubado durante 24-48 horas a 35 °C en agitación a 116 revoluciones por minuto (rpm) en un agitador orbital Innova 4000 (New Brunswick Scientific). Posteriormente a la incubación, se realizó un pase a agar Sabouraud dextrosa (ASD, Oxoid-USA), agar cromogénico (OXOID-USA) y agar mycosel (OXOIDUSA), a fin de verificar la pureza y viabilidad de las cepas seleccionadas, las mismas fueron incubadas a 35°C por 48 horas.
Estudio de la sensibilidad de las cepas en su forma planctónica:
Microdilución en caldo: Para la realización de este método se siguieron las instrucciones del procedimiento descrito por las técnicas de referencia M27 del manual del Clinical Laboratory Standard Institute (CLS por sus siglas en inglés-2017) (12).
Sensibilización de placas para fluconazol: A partir de una solución madre, cuya concentración para fluconazol es de 12.800 mg/ml, se realizaron diez diluciones consecutivas 1:2 utilizando dimetil sulfóxido (DMSO). Posteriormente se realizó una dilución 1:50 en medio RPMI 1640+glucosa al 2% (9,8 ml de RPMI + 0,20 ml de la dilución anterior), para obtener diferentes intervalos de concentraciones. Se inocularon 100 ml de las distintas concentraciones en microplacas estériles de 96 pocillos de fondo en “U”, a partir del pocillo 2 al 11. El pocillo 1 contiene 200 ml de RPMI y el pocillo 12, 100 ml de RMPI. De esta manera, las placas sensibilizadas presentaron las siguientes concentraciones a fluconazol: 64; 32; 16; 8; 4; 2; 1; 0,5; 0,25; 0,125 (mg/mL) (13).
Preparación del inóculo: El inóculo se preparó mediante una suspensión ajustada al 0,5 McFarland, a partir del cultivo puro crecido en 24 h de cada aislamiento en ASD. A partir de esta suspensión se realizó una dilución de 1:100 (9,9 ml de RPMI + 0,1 ml de la suspensión 0,5 McFarland). Posteriormente, las placas previamente sensibilizadas se inocularon con 100 ml de dicha dilución desde el pocillo 2 al 12; el pocillo 1 corresponde al control de esterilidad que contiene 200 ml de RMPI y el pocillo 12, inoculado previamente con 100 ml de RPMI se le agregaron 100 ml de inóculo de la cepa en estudio actuando como control de crecimiento. Las placas se incubaron a 35 °C durante un período máximo de 48 h, la lectura se realizó visualmente a las 24h (13).
Interpretación de las concentraciones mínimas inhibitorias: La lectura del pocillo 1 se consideró como el blanco de la prueba, cuyo valor se comparó con cada una de las lecturas de cada columna. El valor de la concentración mínima inhibitoria (CMI) para los azoles en este caso fluconazol se interpretó como la menor lectura correspondiente a la concentración del fármaco que da lugar a una inhibición de crecimiento menor o igual al 50 % con respecto al pocillo 12, considerado como control de crecimiento (13). Los criterios de interpretación de las pruebas de susceptibilidad siguiendo los puntos de corte clínicos establecidos por el documento CLSI-M27M44S-2022 fueron los siguientes: Sensible (S): ≤ 2 mg/mL, para los Complejos C. albicans y Candida parapsilosis, así como para C. tropicalis excepto el Complejo N. glabrata que no tiene punto de corte clínico para esta categoría; Sensible dosis dependiente (SDD): 4 mg/mL, para los Complejos C. albicans y Candida parapsilosis, así como para C. tropicalis, mientras que para el Complejo N. glabrata es de ≤32 mg/mL, y la categorización Resistente (R): ≥8 mg/mL para los Complejos C. albicans y Candida parapsilosis, así como para C. tropicalis y para el complejo N. glabrata es de ≥ 64 mg/mL (14).
Control de calidad: Como control de calidad de medios, identificación y sensibilidad de las cepas se utilizaron las cepas de American Type Culture Collection (ATCC.): Candida parapsilosis (ATCC 22019), Candida krusei (ATCC 6258). También se utilizaron las cepas (ATCC.): Candida albicans ATCC. 90028, Nakaseomyces glabrata ATCC. 90030, como cepas para valorar su comportamiento con respecto a las cepas valoradas en el estudio.
Estudio de la sensibilidad de las cepas en su forma sésil: La valoración de las cepas en su estado sésil se realizó utilizando la técnica colorimétrica con el indicador de resazurina, tomando en consideración ciertos criterios referenciados por Punithavathy et al. (15) y Shabanzadeh et al. (16) en cuanto a:
Preparación del inóculo: Los aislamientos frescos, puros y viables recuperados en ASD se suspendieron en cloruro de sodio (NaCl) al 0,9 % y la turbidez se ajustó a 0,5 McFarland.
Preparación de la solución madre del colorante resazurina: Se preparó diluyendo la sal sódica de resazurina en agua destilada al 0,01 % (p/v) y se esterilizó por filtración. Se agregó 10 ml a la placa incubada por 72 h luego de haberse formado las biopelículas y haberse agregado las diferentes concentraciones del antifúngico a las placas de poliestireno en una proporción de 1:10 (0,001 %).
Preparación de las concentraciones de fluconazol: A partir de la solución constituida por (RPMI + MOP y 1024 mg de solución madre de fluconazol (en 5 mL de DMSO), se prepararon diferentes concentraciones de fluconazol quedando de la siguiente manera: 1.024; 512; 256; 128; 64; 32; 16; 8; 4; 2 (mg/ml).
Formación de las biopelículas: Utilizando microplacas de poliestireno de fondo plano preesterilizadas, se agregaron 90 ml de caldo Sabouraoud dextrosa (CSD) suplementado con glucosa al 8 %, más 10 ml de las suspensiones celulares preparadas anteriormente, una cepa por cada línea de pocillos horizontales: desde el pocillo 2 hasta el pocillo 12, y se incubaron durante 48 horas a 35 °C ± 2. Una vez formadas las biopelículas, se eliminaron las células planctónicas lavando minuciosamente tres veces con buffer PBS a pH 7,4. Se utilizaron toallas de papel absorbente para eliminar los restos del buffer de la microplaca. El pocillo 1 se dejó sin suspensión celular como control negativo.
Estudio de la sensibilidad de las cepas en su forma sésil: Se añadió asépticamente 200 ml de la dilución correspondiente del agente antifúngico (fluconazol) a cada pocillo correspondiente de la placa de poliestireno con las biopelículas sésiles ya formadas desde el pocillo 2 al pocillo 11 y se incubaron durante 48 horas más a 35 °C ± 2. Posteriormente para detectar la viabilidad de las biopelículas respecto a la dilución correspondiente del antifúngico, se agregó al pocillo 1, 100 ml de la solución RPMI + MOP +10 ml de colorante de resazurina, como control negativo de la prueba, y 10 ml de resazurina a todos los pocillos del estudio, y se reincubaron las placas nuevamente a 35 °C ± 2 por 24 h más.
Interpretación de la CMI de las biopelículas sésiles: La lectura visual se determinó como la concentración más baja del agente antifúngico que mantiene el color azul del medio colorimétrico.
Análisis estadístico: Los datos obtenidos se ordenaron en una tabla de Excel y se determinaron las frecuencias y porcentajes para cada categoría mediante el uso de estadística descriptiva.
Resultados
De las 80 cepas seleccionadas para valorar la utilidad de la resazurina como indicador colorimétrico en la susceptibilidad a biopelículas de Candida spp., aisladas de hemocultivos frente a fluconazol, se seleccionaron cepas formadoras de biopelículas, que ya habían sido analizadas y reportadas en un estudio previo, resultando 10 cepas del Complejo C. albicans : 9 (90 %) formadoras débiles y 1 (10 %) formadora moderada de biopelículas. Once cepas del Complejo C. parapsilosis : 9 (82 %) formadoras débiles y 2 (8 %) formadoras moderadas de biopelículas. Diez de C. tropicalis : 8 (80 %) formadoras débiles y 2 (20 %) formadoras moderadas de biopelículas y 13 del Complejo N. glabrata : 12 (92 %) formadoras débiles y 1 (8 %) formadora moderada de biopelículas. No se encontraron cepas aisladas del torrente sanguíneo con capacidad fuertemente formadora de biopelículas.
Las cepas del Complejo C. albicans en su estado planctónico por la técnica de microdilución en caldo frente a fluconazol, exhibieron CMIs entre 0,125 mg/mL y 0,5 mg/mL; las cepas del Complejo C. parapsilosis en su estado planctónico mostraron CMIs entre 0,125 mg/mL y 0,25 mg/mL y las CMIs exhibidas en las cepas de C. tropicalis mostraron un rango entre 0,125 mg/mL y 0,5 mg/mL, interpretándose todas estas CMIS como sensibles. Finalmente, las CMIs para N. glabrata exhibieron rangos entre 0,5 mg/mL y 16 mg/mL, ubicándose en la categorización de sensible dosis dependiente con concentraciones inferiores a 32 mg/ mL. Ver Figura 1: A1, B1, C1, D1 y Tabla 1. Las cepas controles o ATCC. utilizadas en el estudio, estuvieron dentro de los rangos establecidos ratificando la sensibilidad y especificidad de la prueba.
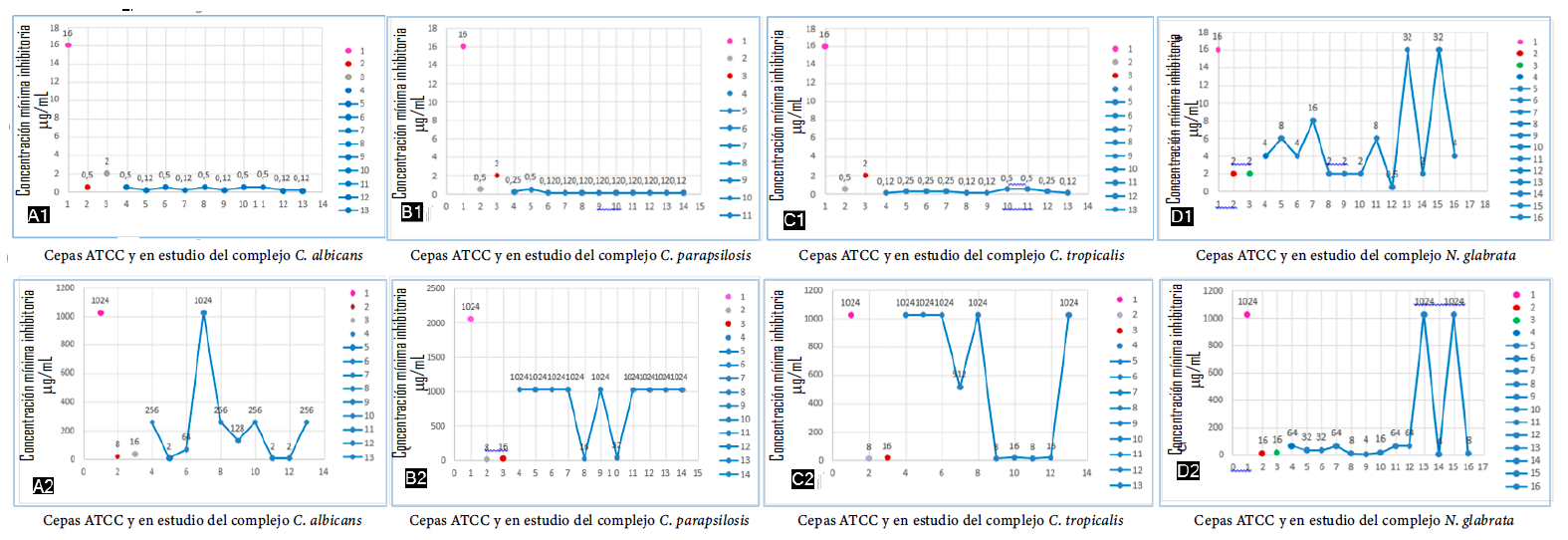
Figura 1. A1, A2: Susceptibilidad in vitro del Complejo Candida albicans en su estado planctónico y sésil por el método de microdilución en caldo frente a fluconazol. Cepas ATCC 1,2,3= Pichia kudriavzevii (Candida krusei) ATCC. 6258, Candida albicans ATCC. 90028, Candida parapsilosis ATCC. 22019. Cepas en estudio 4-13. Figura 1- B1, B2: Susceptibilidad in vitro del Complejo Candida parapsilosis en su estado planctónico y sésil por el método de microdilución en caldo frente a fluconazol. Cepas ATCC 1,2,3= Pichia kudriavzevii (Candida krusei) ATCC. 6258, Candida albicans ATCC. 90028, Candida parapsilosis ATCC. 22019. Cepas en estudio 4-14. Figura 1- C1, C2: Susceptibilidad in vitro de Candida tropicalis en su estado planctónico y sésil por el método de microdilución en caldo frente a fluconazol. Cepas ATCC 1,2,3= Pichia kudriavzevii (Candida krusei) ATCC. 6258, Candida albicans ATCC. 90028, Candida parapsilosis ATCC. 22019. Cepas en estudio 4-13. Figura 1-D1, D2: Susceptibilidad in vitro del Complejo Nakaseomyces glabrata en su estado planctónico y sésil por el método de microdilución en caldo frente a fluconazol. Cepas ATCC 1,2,3= Pichia kudriavzevii (Candida krusei) ATCC. 6258, Candida parapsilosis ATCC..
En el presente estudio el Complejo Candida albicans, documentó marcadas diferencias de las CMIs entre su estado sésil y su estado planctónico, como las observadas en las cepas 11143 y 8459 que fueron 16,67 veces superior en su estado sésil (2 mg/mL) en comparación con su estado planctónico (0,125 mg/mL). De igual manera la cepa 9525, se notó que su CMI fue 2.048 veces mayor en su estado sésil (1.024 mg/mL) al compararse con su estado planctónico (0,5 mg/mL). Además, en la cepa 8856 se obtuvo que esta es 128 veces mayor en su estado sésil. Las CMIs de todos los aislamientos del Complejo C. albicans en su condición planctónica como sésil se aprecian con mayor minuciosidad en las Figuras 1 A1-2, 2 A1-2. Tabla 1 y Tabla 2.
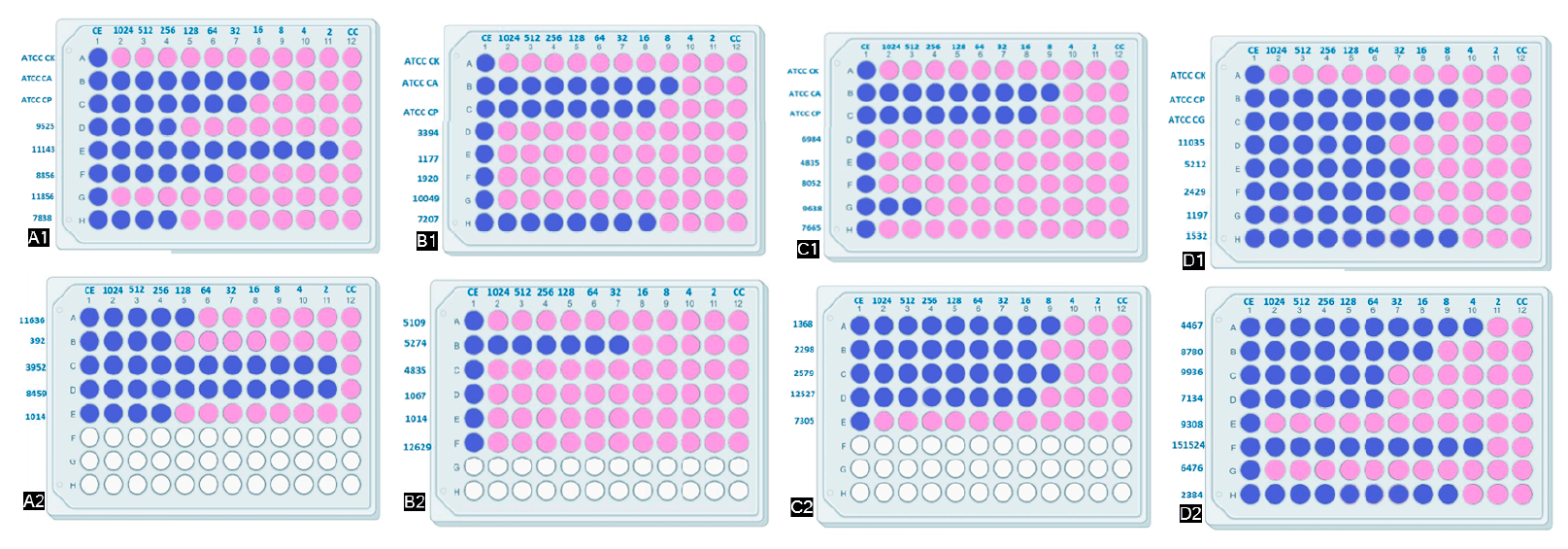
Figura 2. A1, A2, B1, B2, C1, C2, D1, D3: Prueba de coloración con resazurina en placas de poliestireno de 96 pocillos para determinar la concentración mínima inhibitoria a fluconazol en biopelículas del Complejo C. albicans, Complejo C. parapsilosis, C. tropicalis y N. glabrata . El crecimiento en el medio se indica mediante un cambio de color de azul a rosa.
Para el Complejo C. parapsilosis observamos que las CMIs de los aislamientos 10049, 1067, 1014 y 12629 evidenciaron una CMI 17.066,67 veces mayor en su estado sésil (1.024 mg/mL) en comparación al estado planctónico (0,125 mg/mL). Los valores de la CMI para todas las cepas del Complejo C. parapsilosis en su estado planctónico como sésil se pueden ver en las Figuras 1 B1-2, 2 B1-2. Tablas 1 y 2.
Los datos plasmados en las Figuras 1 C1-2, 2 C1-2 y las Tablas 1 y 2 para C. tropicalis en su estado planctónico como sésil, podemos observar, citando ejemplos, que las cepas 4835 y 8052 fueron 4.096 veces mayor en su estado sésil (1.024ug/mL) con respecto a su estado planctónico (0,25 ug/mL). Y para la cepa 9638, ésta fue 2.048 veces mayor en su estado sésil (512ug/mL) con respecto a su estado planctónico (0,25 ug/mL).
Tabla 1.
Distribución de las concentraciones mínimas inhibitorias de las cepas de Candida spp., frente a fluconazol en su estado planctónico por el método de dilución en caldo (n=44)
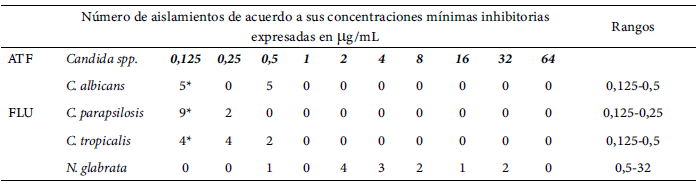
*: Cepas con concentración mínima inhibitoria menor o igual a 0,125; ATF: antifúngico; FLU: fluconazol
Las CMIs realizados para las cepas de N. glabrata arrojaron un aumento significativo de las CMIs, al compararse su estado sésil con su estado planctónico, obteniéndose que las cepas 151524 y 4467 alcanzaron una CMI 2 veces mayor en su estado sésil (4 mg/mL) frente a su estado planctónico (2 mg/mL). Para las cepas 9308 y 6476 se observó que estas fueron 64 veces mayores en su estado sésil (1.024 ug/mL) con respecto a su estado planctónico (32 ug/mL). Y con respecto, a la cepa 11035 arrojó un resultado 16 veces mayor en su estado sésil (64 mg/mL) respecto a su estado planctónico (4 mg/mL). Los valores de las CMIs para todos los aislamientos en su estado plantónico y sésil del Complejo N. glabrata pueden consultarse con mayor detalle en las Figuras 1 D1-2, 2 D1-2. Tablas 1 y 2.
Tabla 2.
Distribución de las concentraciones mínimas inhibitorias de las cepas de Candida spp., frente a fluconazol en su estado sésil por el método de dilución en caldo (n=44)
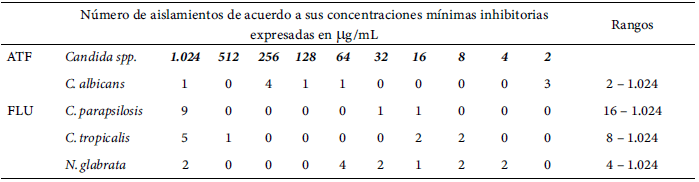
ATF: antifúngico; FLU: fluconazol
Discusión
El uso de dispositivos protésicos como los catéteres se han incrementado en los últimos años, y a su vez se ha observado un aumento notable en el uso de dispositivos intrahospitalarios, y con ello las infecciones por microorganismos formadores de biopelículas. Las especies de Candida son importantes patógenos en las infecciones asociadas con la atención en salud. Por lo tanto, la implantación de estos dispositivos, contribuyen a los factores de riesgo para el desarrollo de la candidiasis invasora (15). Las formas sésiles de las especies de Candida tienden a ser más resistentes a los agentes antifúngicos que sus formas planctónicas. Los mecanismos por los cuales estas formas presentan una mayor resistencia no se comprenden completamente, pero se cree que se deben a mecanismos complejos como la menor difusión de agentes antimicrobianos a través de la capa de biopelícula, una tasa de crecimiento lenta y la expresión de genes resistentes inducida por la superficie (17).
El presente estudio se centró en la evaluación de la susceptibilidad de fluconazol en aislados de Candida spp., obtenidos de hemocultivos, contrastando la respuesta en células planctónicas (libres) con la de las biopelículas (sésiles) mediante la implementación del indicador colorimétrico de resazurina. Los resultados obtenidos en la presente investigación confirman y reafirman que la formación de biopelículas por los hongos en su estado sésil es un factor de virulencia crucial que confiere una marcada resistencia antifúngica, con implicaciones directas para el manejo de la candidemia (2).
Los aislamientos clínicos provenientes de hemocultivos demuestran la importancia continua de las especies de Candida en las infecciones del torrente sanguíneo. Si bien en el estudio no se investigaron la mayoría de las especies de Candida , la inclusión del Complejo Nakaseomyces glabrata , el Complejo C. parapsilosis y C. tropicalis refleja el panorama epidemiológico actual, en el cual las especies de Candida no albicans son patógenos emergentes y a menudo más resistentes a los azoles que C. albicans causantes de candidemias (18).
MinionVariableConcept-Roman; El hallazgo más significativo del proyecto es la alta capacidad de formación de biopelículas en su estado sésil observada en todos los aislados de hemocultivos evaluados (clasificados como productores débiles, moderados o fuertes). Esta capacidad es un prerrequisito para la infección asociada con dispositivos médicos, favoreciendo la instauración de una candidiasis en el torrente sanguíneo (19).
El aumento de la CMI en biopelículas en el presente estudio se ve demostrada cuando las células sésiles incrustadas en el biofilm requieren de una CMI en estado sésil significativamente más alta para ser erradicadas que la CMI de sus contrapartes planctónicas. Esta resistencia es multifactorial, atribuible a la barrera física de la matriz de sustancia polimérica extracelular (EPS), la presencia de bombas de eflujo y el estado fisiológico alterado (lento crecimiento) de las células dentro de la biopelícula (20).
En el estudio realizado por Shabanzadeh et al . se demostró cómo las biopelículas en su estado sésil del Complejo C. albicans eran considerablemente menos susceptibles a caspofungina y luliconazol que las células planctónicas, requiriendo concentraciones del fármaco exponencialmente mayores (16). Sin embargo, en la presente investigación a pesar de que no se utilizó caspofungina y luliconazol, sino fluconazol, se demostró de igual forma que se requieren concentraciones del fármaco más altas ante la formación de biopeliculas en su estado sésil, en comparación a su estado planctónico, donde el 50 % de las cepas del Complejo C. albicans tenían un CMI de 0,5 mg/mL en su estado planctónico, mientras que en su estado sésil el 70% de las cepas mostraron una CMI extremadamente alta, distribuyéndose de la siguiente manera: el 40 % tuvo una CMI mayor a 256 mg/mL, el 10 % alcanzó los 1.024 mg/mL, y el 20 % restante presentó CMI de 128 mg/mL y 64 mg/mL, distribuidos en un 10 % respectivamente. El 30 % restante de las cepas sésiles tuvo una CMI de 2 mg/mL. Se destaca también como la cepa 11856 de C. albicans en el presente estudio fue 8.533,33 veces mayor su CMI en su estado sésil (1.024mg/mL) en comparación con la CMI en su estado planctónico (0,125 mg/mL), lo que nos indica la CMI máxima que se pudiera utilizar para inhibir el crecimiento en su estado sésil.
De manera similar, Punithavathy et al ., observaron un aumento de la resistencia a fluconazol en las biopelículas en estado sésil de C. tropicalis en comparación con las CMI planctónicas, confirmando la generalidad de este fenómeno (15).
En el presente estudio se evidenció que el 40 % de las cepas formadoras de biopeliculas en su estado planctónico de C. tropicalis proyectaron una CMI de 0,25 mg/mL y en el caso de las sésiles el 50 % presento una CMI de 1.024mg/mL. Y citando como ejemplo las cepas 9984 y 7305 fueron 8.533,33 veces mayores las CMI en su estado sésil (1.024 mg/mL) con respecto a las CMI en su estado planctónico (0,125 mg/mL), queriendo decir que se necesita una CMI de 1.024 mg/mL para inhibir el crecimiento en su estado sésil.
En la literatura revisada no se encontró la aplicabilidad del uso de la resazurina como validante de la viabilidad y CMI en el complejo C. parapsilosis y N. glabrata . Sin embargo, en el presente estudio de investigación el complejo N. glabrata no presentó CMI tan elevadas en su estado sésil respecto a las CMI en su estado planctónico. La mayor CMI fue en la cepa 7134 quien fue 128 veces mayor la CMI en su estado sésil (64 mg/mL) con respecto a su estado planctónico (0,5 mg/mL), por lo que se necesita una CMI de 64 mg/ mL para erradicar la biopelícula en su estado sésil, esto pudiera deberse al comportamiento de cada especie de Candida.
Finalmente, al analizar el complejo C. parapsilosis tampoco se obtuvo referencia de otros estudios con la misma metodología utilizada, pero tomando en cuenta los resultados obtenidos tenemos que en el caso de las cepas 7207, 5109 y 4835, estas fueron 34.133,33 veces mayor la CMI en su estado sésil (1.024 mg/mL), respecto a las CMI que en su estado planctónico (0,125 mg/mL), donde las CMI necesaria requerida para erradicar la biopelícula es de 1.024 mg/mL en su estado sésil.
Con respecto a la resazurina, la validación de esta como indicador colorimétrico para la determinación de la formación de biopeliculas representa un avance metodológico clave en esta investigación, ya que la medición de la viabilidad metabólica de la resazurina es crucial, a diferencia del Cristal Violeta (que solo mide la biomasa total) o la lectura visual de turbidez, por lo tanto, la resazurina evalúa la viabilidad metabólica de las células. La conversión del colorante azul a resorufina (rosa o incoloro) es un marcador directo de las células fúngicas activas o viables.
En otro contexto la eficiencia y bajo costo de la resazurina demostró ser un método rápido, económico y reproducible para determinar el punto final de inhibición en las biopelículas sésiles, proporcionando una alternativa viable a métodos más costosos como el XTT o el MTT (9). La inclusión de la resazurina en la metodología de pruebas de susceptibilidad no solo mejora la precisión diagnóstica al medir la CMI en el estado sésil, sino que también ofrece a los laboratorios clínicos una herramienta de fácil acceso para evaluar el verdadero potencial patogénico de los aislamientos de Candida spp. en el contexto de las infecciones asociada con la formación de biopelículas (6).
Conclusión
Se concluye que la presencia de biopelículas en su estado sésil en aislados de Candida s pp. d e hemocultivos impone un fenotipo de resistencia significativa al fluconazol que no se detectaría con las pruebas de susceptibilidad planctónicas estándar. Además, la validación exitosa de la resazurina para la determinación de la CMI en el estado sésil ofrece una ruta para implementar pruebas de susceptibilidad a biopelículas en la práctica clínica, lo cual es fundamental para optimizar el tratamiento de la candidemia y reducir las altas tasas de mortalidad asociadas a la resistencia antifúngica.
Declaración financiamiento y conflictos de interés
El presente trabajo de investigación fue financiado con recursos del Laboratorio de la Cátedra de Bacteriología y Micología de la Escuela de Bioanálisis “Dr. Rafael Rangel-UCV, Dpto. de Micología del Instituto Nacional de Higiene Rafael Rangel y fondos propios de los investigadores. Los autores declaran que no existe ningún conflicto de intereses que pueda influir en la honestidad o integridad de la publicación.
Referencias
- Castrillon Rivera LE, Palma Ramos A, Padilla Desgarennes MDC. Biopeliculas fungicas. Dermatol Rev Mex 2013;57(5):350-361. [cited 2 Oct. 2025]. Disponible en: http://scielo.sld.cu/scieloOrg/php/reflinks.php?refpid=S1029-3043201600030000200021&lng=pt&pid=S1029-30432016000300002
- Del Pozo JL, Canton E. Candidiasis asociada a biopeliculas Infecciones relacionadas con biopeliculas de Candida. Rev Iberoam Micol 2016;33(3):176-183. https://doi.org/10.1016/j.riam.2015.06.004
- Trelles M, Murillo J, Fuenmayor-Gonzalez L, Yu-Liu Y, Alexander-Leon H, Acebo J, et al . Prevalencia de infecciones fungicas invasivas en pacientes criticos: una revision sistematica y un metaanalisis. BMC Infect Dis 2025;25(1):896. https://doi.org/10.1186/s12879-025-11264-z
- Trevino Rangel RJ, Pena Lopez CDP, Hernandez Rodriguez PA, Beltran Santiago D, Gonzalez GM. Association between Candida biofilm-forming bloodstream isolates and the clinical evolution in patients with candidemia: An observational nineyear single center study in Mexico Rev Iberoam Micol 2018;35(1):11-16. https://doi.org/10.1016/j.riam.2017.01.005
- Amann V, Kissmann AK, Firacative C, Rosenau F. Biofilm-Associated Candidiasis: Pathogenesis, Prevalence, Challenges and Therapeutic Options. Pharmaceuticals (Basel). 2025;18(4):460. https://doi.org/10.3390/ph18040460
- Van den Driessche F, Rigole P, Brackman G, Coenye T. Optimization of resazurin-based viability staining for quantification of microbial biofilms. J Microbiol Methods. 2014;98:31-34. https://doi.org/10.1016/j.mimet.2013.12.011
- Lopez Avila K, Dzul Rosado KR, Lugo Caballero C, Arias Leon JJ, y Zavala Castro JE. Mecanismos de resistencia antifungica de los azoles en Candida albicans . Una revision. Revista Biomedica. 2016;27(3):127-136. [cited 2 Oct. 2025]. Disponible en: http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S2007-84472016000300127&lng=es
- Valentin A, Canton E, Peman J, Quindos G. In vitro activity of amphotericin B and anidulafungin against Candida spp biofilms. Rev Iberoam Micol. 2007;24(4):272-277. https://doi.org/10.1093/jac/dkw316
- Esteves Barros IL, Franco Veiga F, Luiz Correa J, Carrilho Jarros I, Negri M, Estivalet Svidzinski TI. Standardization of resazurin use in susceptibility testing of natural products against yeasts in planktonic cells and in biofilms formation. Act Scient Biol Scien 2021;43:e55700. https://doi.org/10.4025/actascibiolsci.v43i1.55700
- Castellani A. Further researches on the long viability and growth of many pathogenic fungi and some bacteria in sterile distilled water. Mycopathol Mycol Appl 1963;20:1-6. https://doi.org/10.1007/BF02054872
- Moreno X, Ventura M, Panizo MM, Garces MF. Evaluacion de la formacion de biopeliculas en aislamientos bacterianos y fungicos por los metodos semicuantitativo de microtitulacion con cristal violeta y cualitativo de agar con rojo Congo. Biomedica. 2023;43(Supl.1):77-88. https://doi.org/10.7705/biomedica.6732
- CLSI. Reference Method for broth dilution antifungal susceptibility testing of yeast. 4th ed. CLSI Standard M27 [Electronic]. Clinical and Laboratory Standards Institute; 2017.
- Manuel Cuenca-Estrella M, Rodriguez-Tudela JL. Metodo estandarizado por el EUCAST para el estudio de la sensibilidad a los antifungicos En: J Peman, E Martin-Mazuelos, MC Rubio Calvo. Identificacion y Diagnostico en Micologia Clinica. 2da ed. Bilbao 2007. [cited 2 Oct. 2025]. Disponible en: https://www.researchgate.net/publication/269399286_Metodos_estandarizados_por_el_EUCAST_para_el_estudio_de_la_sensibilidad_a_los_antifungicos_documento_71
- CLSI. Performance Standars for Antifungal Susceptibility Testing of Yeast. 3rd ed. CLSI suplement M27M44S [Electronic]. Clinical and Laboratory Standards Institute; 2022.
- Punithavathy PM, Nalina K, Menon T. Antifungal susceptibility testing of Candida tropicalis biofilms against fluconazole using calorimetric indicator resazurin. Indian J Pathol Microbiol 2012;55(1):72-74. https://doi.org/10.4103/0377-4929.94861
- Shabanzadeh M, Rezaei-Matehkolaei A, Zarei Mahmoudabadi A. The efficacy of luliconazole and caspofungin on planktonic and biofilm of Candida albicans from different sources. Iranian J Microbiol 2025;17(4):653-659. https://doi.org/10.18502/ijm.v17i4.19261
- Araujo D, Henriques M, Silva S. Portrait of Candida species biofilm regulatory network genes. Trends Microbiol 2017;25(1):62-75. https://doi.org/10.1016/j.tim.2016.09.004
- Salmanton-Garcia J, Cornely OA, Stemler J, Bara. A, Steinmann J, Sivakova A, et al . Attributable mortality of candidemia Results from the ECMM Candida III multinational European Observational Cohort Study. J Infect 2024;89(3):106229. https://doi.org/10.1016/j.jinf.2024.106229
- Quindos G. Epidemiologia de las micosis invasoras: un paisaje en continuo cambio. Rev Iberoam Micol 2018;35(4):171-178. https://doi.org/10.1016/j.riam.2018.07.0021130-1406
- Costa-Orlandi CB, Sardi JCO, Pitangui NS, de Oliveira HC, Scorzoni L, Galeane MC, et al . Fungal Biofilms and Polymicrobial Diseases. J Fungi (Basel) 2017;3(2):22. https://doi.org/10.3390/jof3020022
