Introducción
Staphylococcus aureus (S. aureus) es un coco Grampositivo que se dispone en tétradas y racimos de uvas y entre otras de sus características resaltan ser no esporulados, inmóviles, catalasa positivos y facultativamente anaeróbicos (1). Por otra parte, S. aureus tiene la habilidad de desarrollar resistencia a los antibióticos, siendo las cepas de S. aureus resistente a la meticilina (SARM) de gran importancia clínica por sus limitadas opciones de tratamiento antimicrobiano (2).
Esta bacteria es catalogada como un patógeno exitoso, ya que cuenta con una serie de factores de virulencia, entre ellos su capacidad de adherencia a las células del huésped, la evasión de la respuesta inmune, la degradación y adquisición de nutrientes. Por otra parte, posee una maquinaria genética involucrada en la síntesis de una variedad de enzimas y toxinas como proteasas, hialuronidasas y hemolisinas que forman parte de su abanico de estrategias para sobrevivir ante los mecanismos defensivos del hospedador (3).
Las infecciones por S. aureus pueden originarse a partir de la colonización en diferentes sitios del cuerpo (fosas nasales, piel e intestino), por heridas en la piel o también a partir de fómites infectados, contaminación de dispositivos médicos implantables (catéteres, prótesis) o por transferencia de otros individuos, condiciones que se dan principalmente en ambientes hospitalarios relacionados con la atención en salud (2).
En ese sentido, S. aureus es el agente causal de múltiples infecciones humanas, en la comunidad y a nivel hospitalario, que incluyen bacteriemia, endocarditis infecciosa, infecciones de piel y tejidos blandos, osteomielitis, artritis séptica, infecciones de dispositivos protésicos, infecciones pulmonares (neumonía y empiema), gastroenteritis, meningitis, síndrome de shock tóxico e infecciones del tracto urinario (4).
Se ha estimado que la bacteriemia por S. aureus tiene una tasa de incidencia que varía de 20 a 50 casos/100.000 por año, y entre el 10% y el 30% de estos pacientes morirán a causa de la infección (5,6). En Estados Unidos se producen aproximadamente 20.000 muertes por año por bacteriemia por esta bacteria (5,6). Asimismo, las infecciones cutáneas pueden ser moderadamente graves, e incluyen furúnculos, abscesos e infecciones de heridas, y aunque no suelen ser mortales, están acompañadas de una morbilidad significativa (1).
Staphylococcus aureus se encuentra entre los siete patógenos principales que son responsables de aproximadamente 457.000 muertes relacionadas con resistencia a los antimicrobianos (RAM) en 53 países europeos, siendo SARM la causa predominante. Asimismo, SARM ocasionó más de 100.000 muertes en el mundo atribuibles a la RAM en 2019 (7). Según la Organización Mundial de la Salud (OMS), SARM se encuentra entre los patógenos de prioridad alta por su resistencia a los antibióticos (8).
En Venezuela, según el Programa Venezolano de Vigilancia de la Resistencia a los Antimicrobianos (PROVENRA), entre los años 2018 al 2020 se estimó un alto porcentaje de RAM en S. aureus , siendo de 51,7 % SARM, mientras que 47% de cepas se reportaron como resistentes a eritromicina y 67,32 % a azitromicina (9).
La pandemia de COVID-19 fue uno de los eventos más impactantes que estremeció al mundo desde su aparición en la ciudad de Wuhan, China, en diciembre de 2019. Se propagó rápidamente y se inició el 11 de marzo de 2020. La pandemia COVID-19 marcó un antes y un después en el planeta, con graves consecuencias en los aspectos políticos y socioeconómicos, y provocó una crisis sanitaria sin precedentes con la aparición adicional de otras enfermedades y complicaciones debidas al SARS-CoV-2 (10,11).
En ese mismo contexto, se observó una alta frecuencia de coinfección de SARS-CoV-2 con otros patógenos respiratorios bacterianos en pacientes ingresados en los centros de salud, entre los más comunes se reportaron S. aureus y K. pneumoniae complex, lo que obligó al uso sistemático de antibióticos en casos graves y complicados de neumonía, así como el uso excesivo de fluorquinolonas (12). Aunado a esto, los macrólidos se utilizaron como farmacoterapia en pacientes con COVID-19 por su efecto antiinflamatorio (13). Todos estos elementos, sumado a la automedicación y el uso irracional de antibióticos, exacerbaron la propagación de la resistencia a estos fármacos (12,13).
En efecto, diversos estudios han reportado que la pandemia de COVID-19 coincidió con cambios en la epidemiología y los patrones de RAM de varios patógenos humanos que incluyeron S. aureus (14-16). En tal sentido, Ai et al . en un estudio retrospectivo de infecciones en pacientes pediátricos con neumonía adquirida en la comunidad, antes (de 2018 a 2019) y durante (de 2020 a 2022) de la pandemia de COVID-19, observaron que en S. aureus aumentó la resistencia a la oxacilina y la tetraciclina (15).
En Venezuela no hay reporte de cifras oficiales relacionadas con la RAM durante la COVID-19, razón por la cual resulta importante determinar cómo la pandemia influyó en la resistencia a antibióticos de S. aureus , de manera de optimizar el uso de antibióticos en los centros asistenciales. En tal sentido, el objetivo de esta investigación fue evaluar el impacto de la pandemia COVID-19 en la resistencia a los antimicrobianos en Staphylococcus aureus en el estado Aragua- Venezuela, en el periodo 2019 al primer trimestre del 2024, correspondiente a antes, durante y después de la pandemia. Para tal efecto, se identificaron los cultivos de muestras clínicas positivos para S. aureus según el año y tipo de muestra, se determinó las resistencias a Meticilina, macrólidos, lincosamidas y fluorquinolonas, y se comparó la variación de la resistencia antimicrobiana de S. aureus en los años de estudio.
Materiales y métodos
Tipo de investigación
La investigación es de tipo descriptiva, retrospectiva y de corte transversal.
Población y Muestra
La población estuvo conformada por las muestras clínicas de todos aquellos pacientes que fueron referidos al Departamento de Microbiología del Laboratorio Clínico Delgado Launois en el periodo 2019-2024. El muestreo fue de tipo intencional no probabilístico. La muestra estuvo representada por los cultivos de las muestras clínicas que resultaron positivos a S. aureus.
Procedimiento
Los datos de los cultivos, identificación y resistencia a antimicrobianos se obtuvieron de los cuadernos de registro de los cultivos del Departamento Microbiológico en el laboratorio Clínico Delgado Launois, durante el periodo 2019-2024. Se obtuvo la autorización de la junta directiva de este centro de salud, con el compromiso de mantener la confidencialidad de la información de los pacientes y dejando por sentado que los datos serían utilizados solo para efectos de esta investigación.
Se utilizó una hoja de registro digital diseñada en el programa Microsoft Excel 2010, que permitió ordenar y clasificar los datos de los pacientes y los resultados obtenidos del análisis de los cultivos bacterianos según las variables de estudio: año (2019: antes de la pandemia, 2020 al 2022: durante la pandemia y 2023 al primer trimestre del 2024: después de la pandemia), tipo de muestra, resultado del cultivo y resistencia fenotípica de S. aureus a: eritromicina, clindamicina, ciprofloxacina, levofloxacina y meticilina.
La identificación de S. aureus y las resistencias fenotípicas se determinaron en el laboratorio con Vitek 2 compact y/o los métodos convencionales y el método de Kirby-Bauer, en el que la resistencia a meticilino, clindamicina-eritromicina y fluorquinolonas se midieron con los disco de cefoxitina (FOX:30 μg), clindamicina (CC: 2 μg) y eritromicina (E: 15 μg) (junto con la prueba de inducción de clindamicina para la detección de fenotipos inducibles y constitutivos), ciprofloxacina (CIP: 5 μg) y levofloxacina (LEV: 5 μg), de la marca mast group, respectivamente.
Análisis estadístico
Se calcularon las distribuciones de frecuencia absolutas y relativas (%) para las variables cualitativas y se construyeron los intervalos al 95% de confianza para las frecuencias relativas (IC95%). Se cruzaron las variables cualitativas y categorizadas con los años del período considerado para construir las tablas de contingencia correspondientes, sobre éstas se aplicó la prueba de homogeneidad de chi-cuadrado (χ2) para detectar asociaciones entre pares de variables. El nivel de significación se fijó en 5%, por lo que un resultado se consideró estadísticamente significativo si p≤0,05. Los datos se procesaron con los programas estadísticos EPI INFO 7.2.5 (frecuencias absolutas y relativas e intervalos al 95% de confianza para las frecuencias relativas), y SPSS 27.0 (prueba de homogeneidad de χ2).
Resultados
De un total de 11002 cultivos positivos, 1249 (11,4 %), IC95 %= (10,8-11,9 %), fueron positivos para S. aureus. El mayor porcentaje de aislamientos fue en el año 2019 (31,1 %), seguido del año 2022 (19,2 %). No hubo diferencia estadísticamente significativa en la distribución de S. aureus entre los años de estudio (χ2=3,69; p=0,595). Staphylococcus aureus se aisló principalmente de muestras de secreciones, seguido de hemocultivos, con 75,9 % y 12,1 %, respectivamente. (Tabla 1).
Tabla 1.
Frecuencia de aislamiento de Staphylococcus aureus, distribución por año y según tipo de muestra durante el periodo de estudio 2019-2024
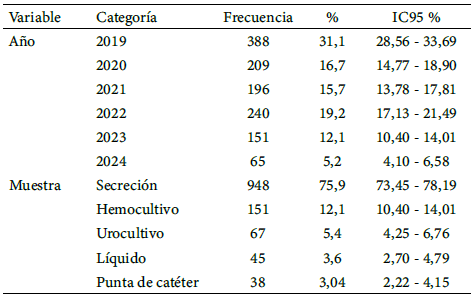
IC: Intervalo de confianza
El 65 % (IC95 %= 62,32 %-67,61 %) de los aislados fue resistente a meticilina. Se observó que el más alto porcentaje de cepas SARM fue en el año 2024 (80 %), seguido del 2023 y 2021 con 76,8 % y 70,9 2019-2024%, respectivamente. La diferencia entre los años de estudio fue estadísticamente significativa (p <0,001) (Tabla 2).
Tabla 2.
Frecuencia de cepas de S. aureus con resistencia a meticilina distribuidos entre los años de estudio 2019-2024
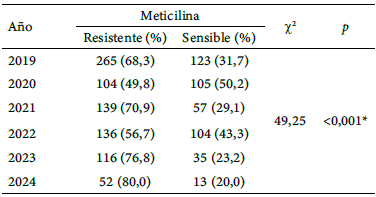
(*) Asociación estadísticamente significativa al 5%
El 50,5 % (IC95 %: 47,8 - 53,3) y 29,9 % (IC95 %: 27,4 - 32,5) del total de aislados de S. aureus fueron resistentes a eritromicina y clindamicina, respectivamente. En la resistencia a eritromicina, se observa un incremento respecto al año 2019 durante la pandemia (2020, 2021 y 2022 de 47,4 %, 50,5 % y 50 %, respectivamente). En la postpandemia fue mayor en el año 2023, seguido de 2024 con 70 % y 67,7 %, respectivamente (Figura 1A). Para la clindamicina, se observaron fluctuaciones en las frecuencias de cepas resistentes durante los años de estudio. Sin embargo, los incrementos más marcados fueron en el año 2024 en el cual hubo mayor resistencia (42 %), seguido del 2022 (37 %) y 2023 (34 %) (Figura 1B). Las diferencias interanuales en ambos casos fueron estadísticamente significativas (p <0,001).
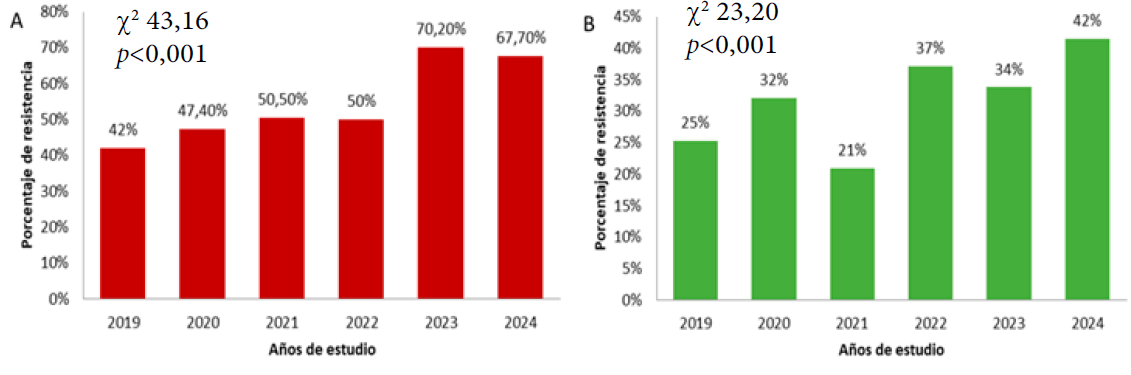
Figura 1. Resistencia a antibióticos (eritromicina y clindamicina) de S. aureus durante el periodo de estudio. La diferencia interanual fue estadísticamente significativa p<0,001. A: Resistencia a eritromicina. B: Resistencia a clindamicina. (χ2): chi-cuadrado. p: Valor probabilístico
Relacionado con los mecanismos de resistencia de los macrólidos y lincosamidas, se observó que la metilasa inducible tuvo un comportamiento ascendente, siendo los años 2022 al 2024 de 15,8 %, 10,6 % y 18,5 %, respectiva y estadísticamente significativos (X2 = 20,98; p <0,001) (Tabla 3). Por su parte, para la resistencia constitutiva se observaron ligeras variaciones que fueron mayores en los años 2022, 2023 y 2024 de 22,5 %, 23,2 % y 23,1 %, respectivamente, con significancia estadística (X2 = 10,68; p =0,060) (Tabla 3). En el caso del Fenotipo M, su mayor frecuencia se observó en el año 2021 (29,6 %), 2023 (36,4 %) y 2024 (26,2 %) y estadísticamente significativo (X2 = 52,4; p >0,001) (Tabla 3).
Tabla 3.
Frecuencia de cepas de S. aureus de acuerdo con la expresión a metilasa inducible, constitutivo y fenotipo M distribuidos entre los años de estudio 2019-2024
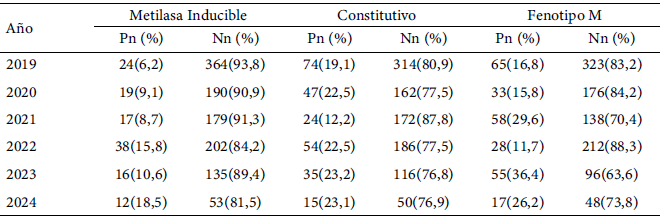
P: Positivo, N: Negativo
En el caso de la resistencia a ciprofloxacina, el 31,6 % (IC95 %: 29,11 - 34,26) de los aislados fueron resistentes. Los mayores porcentajes de resistencia fueron en los años 2023, 2024 y 2022 con 51 %, 45 % y 34 %, respectivamente (Figura 2A). Respecto a levofloxacina, la resistencia fue del 28,6 % (IC95 %:26,15 - 31,15) y en el año 2023 y 2024 se observó el mayor incremento, en 51 % y 45 %, respectivamente (Figura 2B). Las diferencias interanuales en ambos casos fueron estadísticamente significativas (p <0,001).
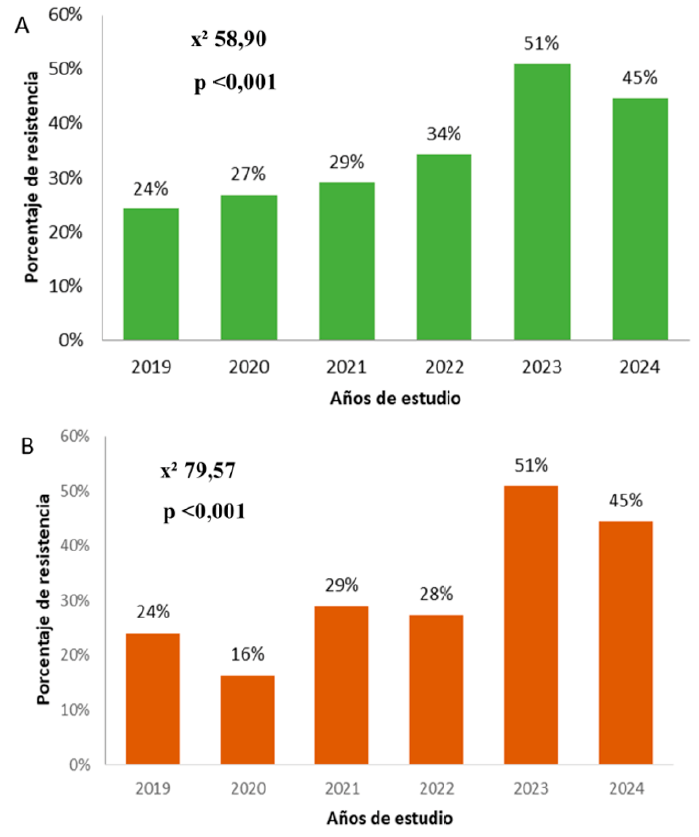
Figura 2. Resistencia a Fluorquinolonas de S. aureus durante el periodo de estudio. La diferencia interanual fue estadísticamente significativa p<0,01. A: Resistencia a ciprofloxacina. B: Resistencia a levofloxacina. (χ2): chi-cuadrado. p: Valor probabilístico
Discusión
La capacidad de S. aureus de desarrollar resistencia a los antimicrobianos limita y dificulta el tratamiento de las infecciones producidas por este microorganismo, lo que obliga a establecer una vigilancia permanente. Durante la pandemia COVID-19 hubo uso indiscriminado de antibióticos, lo que pudo desencadenar cambios en los patrones de resistencia de S. aureus.
En la presente investigación se obtuvieron 1249 cepas de S. aureus, que representó 11,4 % durante el periodo de estudio, un porcentaje menor respecto a investigaciones previas. En ese sentido, Tubaro e t a l. en el 2024 en infecciones de piel y tejidos blandos (IPTB) reportaron una frecuencia de 36,2 % en 6 años de estudio (17). Por su parte, Worku et al . en el 2025 encontraron que S. aureus fue responsable del 26,2 % de los hemocultivos positivos en un estudio retrospectivo de 1 año (18). Ahmet et al . (19) localizaron en un hospital en la ciudad de Makka una frecuencia de S. aureus de 35, 5% en el 2019 y 16 % en el 2020. Sin embargo, Zhao et al . (20) en un estudio de cuatro años (2020-2023) hallaron cifras próximas (1400 aislados), cercanos con los hallazgos de este estudio.
Las diferencias pueden ser atribuibles a que en la presente investigación el análisis se hizo con una amplia variedad de muestras, mientras que los estudios citados se limitaron a analizar muestras de IPTB y hemocultivos. Por otra parte, un porcentaje de las muestras fueron referidas de instituciones hospitalarias y posiblemente no hayan cumplido con los estándares de transporte y preservación, lo que pudo comprometer la viabilidad del microorganismo y afectar los resultados. Adicionalmente, S. aureus se aisló principalmente de muestras de secreciones, seguido de hemocultivos, y estos resultados coinciden con los hallazgos de Tubaro et al. En el 2024 (17), Worku et al. 2025 (18) y Zhao et al. 2024 (20).
Respecto a la resistencia a meticilino, en esta investigación, el porcentaje de SARM fue superior (65,01 %) a lo reportado por Ai et al. (15) en el 2024 (23,1 %) en pacientes pediátricos con neumonía adquirida en la comunidad y Gauto et al. (21) en Argentina, quienes observaron 30 % de resistencia.
Por otra parte, los resultados del presente estudio arrojaron un incremento marcado en la resistencia a meticilino en los años 2021 (pandemia), 2023 y 2024 (postpandemia) con una significancia estadística (p <0,05), similar a la encontrada por Ai et al . quienes reportaron un incremento en la resistencia a este antibiótico para ese periodo (15). Asimismo, Gauto et al. (21) y Zhao et al. (20) observaron ligeros aumentos de la resistencia a la meticilina durante y después de la pandemia sin significancia estadística (p >0,05). Por su parte, López-Jacome et al. (22) demostraron el incremento marcado en la resistencia a la meticilina de 15,2 % en prepandemia (2019) a 36,9 % en la pandemia (2020). A diferencia de los hallazgos de esta investigación y los anteriormente presentados en otros estudios, no se observó incremento en la resistencia a la meticilina durante y posterior a la pandemia COVID-19 (19, 23, 24).
Referente a la resistencia a la eritromicina se observó un incremento postpandemia (2023-2024) entre 70,2 % y 67 %, respecto a los años prepandemia (2019) y pandemia (2020-2022) con una significancia estadística (p <0,001). Los hallazgos son consistentes con lo reportado por López-Jácome et al . (22) en México, quienes observaron un aumento de la resistencia a la eritromicina de 25,7 % en prepandemia a 42, 8% postpandemia con una significancia estadística (p <0,05). El incremento en el aumento de resistencia a eritromicina podría estar asociado a que durante la pandemia los macrólidos se utilizaron de manera indiscriminada en pacientes con COVID-19 por su efecto antiinflamatorio (13).
Sin embargo, contrario a estos resultados, Zhao et al. (20) no encontraron variaciones en la resistencia a eritromicina en Taiwan durante los años 2020, 2021, 2022 y 2023. Por su parte, Golli et al. (24) observaron una disminución de la resistencia a eritromicina postpandemia (55,58 %) respecto a la prepandemia (74,17 %) en la unidad de cuidados intensivos en un hospital de Rumania.
Respecto a la resistencia a las Lincosamidas (clindamicina), se observaron fluctuaciones en los años de estudio, pero en todos los casos fue superior a la prepandemia (2019) y estadísticamente significativo (p <0,001). Los hallazgos son consistentes con los resultados reportados por López-Jácome et al. (22) en México, quienes observaron un aumento de la resistencia a clindamicina de 24,8 % en prepandemia a 43,3 % postpandemia con una significancia estadística (p <0,05). Contrario a estos resultados, Zhao et al. (20) y Golli et al. (24) no encontraron incremento de la resistencia a este antibiótico durante y posterior a la pandemia COVID-19.
En el caso de las fluorquinolonas (ciprofloxacina y levofloxacina) se encontró un aumento en la resistencia durante y posterior a la pandemia. Sin embargo, a diferencia de los hallazgos de esta investigación, estudios previos reportaron que no hubo variaciones en los porcentajes de resistencia a las fluorquinolonas (20, 24).
Las marcadas diferencias observadas en la resistencia de eritromicina, clindamicina y fluorquinolonas respecto a los estudios de Zhao et al. (20) y Golli et al. (24) podrían deberse a que hubo mejores medidas de control respecto al suministro de antibióticos. En nuestra región, la automedicación antimicrobiana, la administración empírica de antibióticos y su uso indiscriminado probablemente fueron los factores detonantes del incremento de la resistencia a antibióticos observada en este estudio durante y posterior a la pandemia COVID-19 (16).
Aunque el estudio tuvo algunas limitaciones por el hecho de ser retrospectivo, con ausencia de datos como la procedencia de los aislados, bien sea de pacientes hospitalizados o de la comunidad, la edad y el género, representa un importante punto de partida para una evaluación más amplia del impacto de la pandemia de COVID-19 en la resistencia a los antimicrobianos en Venezuela.
Finalmente, los hallazgos permitieron concluir que la pandemia COVID-19 tuvo un impacto importante en los aislados clínicos de S. aureus en el estado Aragua, ya que se observó una tendencia significativamente creciente en la tasa de resistencia a los antimicrobianos en el período durante y posterior a la pandemia de COVID-19 para meticilina, clindamicina, eritromicina y fluorquinolonas. Los resultados obtenidos ponen de relieve la necesidad de concienciar al personal médico sobre el uso prudente de los antibióticos y de intensificar las medidas de prevención y control, lo que permitirá limitar la circulación y propagación de patógenos multirresistentes.
Se recomienda el desarrollo de estudios multicéntricos adicionales, que incluyan hospitales territoriales y se extienda a otras regiones del país, que además de S. aureus , abarque otros patógenos de importancia clínica, lo que podría proporcionar datos más precisos sobre el impacto de la pandemia COVID-19 en la resistencia a antimicrobianos y del problema de la resistencia a los antimicrobianos y su impacto en el país, y así poder proponer medidas de contención y control ante la transmisión de la resistencia bacteriana.
Agradecimientos
A la Escuela de Bioanálisis de la Universidad de Carabobo-Núcleo Aragua, al personal del Departamento de Microbiología del Laboratorio Clínico Delgado Launois.
Conflicto de Intereses
Los autores declaramos no tener conflictos de interés.
Financiamiento
El estudio fue autofinanciado.
Referencias
- Cheung GYC, Bae JS, Otto M. Pathogenicity and virulence of Staphylococcus aureus. Virulence 2021;12(1):547-569. https://doi.org/10.1080/21505594.2021.1878688
- Turner NA, Sharma-Kuinkel BK, Maskarinec SA, Eichenberger EM, Shah PP, Carugati M, et al . Methicillin-resistant Staphylococcus aureus: an overview of basic and clinical research. Nat Rev Microbiol 2019;17(4):203-218. https://doi.org/10.1038/s41579-018-0147-4
- Shettigar K, Murali TS. Virulence factors and clonal diversity of Staphylococcus aureus in colonization and wound infection with emphasis on diabetic foot infection. Eur J Clin Microbiol Infect Dis 2020;39(12):2235-2246. https://doi.org/10.1007/s10096-020-03984-8
- Taylor TA, Tobin EH, Unakal CG. Staphylococcus aureus Infection. In StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; USA, 2025. [cited 30 Sep. 2025]. Disponible en: http://www.ncbi.nlm.nih.gov/books/NBK441868/
- van Hal SJ, Jensen SO, Vaska VL, Espedido BA, Paterson DL, Gosbell IB. Predictores de mortalidad en bacteriemia por Staphylococcus aureus. Clin Microbiol Rev 2012;25(2):362.386. https://doi.org/10.1186/s12941-016-0122-8
- McCaig LF, McDonald LC, Mandal S, Jerniganet D. Infecciones de piel y tejidos blandos asociadas a Staphylococcus aureus en atencion ambulatoria. Emerg Infect Dis 2006;12(11):1715.1723. https://doi.org/10.3201/eid1211.060190
- Antimicrobial Resistance Collaborators. Global burden of bacterial antimicrobial resistance in 2019: a systematic analysis. Lancet. 2022;399(10325):629-655. https://doi.org/10.1016/S0140-6736(21)02724-0
- Organizacion Mundial de la Salud. WHO bacterial priority pathogens list, 2024: Bacterial pathogens of public health importance to guide research, development and strategies to prevent and control antimicrobial resistance. [cited 30 Sep. 2025]. Disponible en: https://www.who.int/publications/i/item/9789240093461
- Programa Venezolano de Vigilancia de la Resistencia a los Antimicrobianos [cited 30 Sep. 2025]. Disponible en: https://provenra.com.ve/
- Umakanthan S, Sahu P, Ranade AV, Bukelo MM, Rao JS, Abrahao-Machado LF, et al . Origin, transmission, diagnosis and management of coronavirus disease 2019 (COVID-19). Postgrad Med J 2020;96(1142):753-758. https://doi.org/10.1136/postgradmedj-2020-138234
- Organizacion Mundial de la Salud. La OMS caracteriza a COVID-19 como una pandemia. 2020. [Internet]. [cited 30 Sep. 2025]. Disponible: https://www.paho.org/es/noticias/11-3-2020-oms-caracteriza-covid-19-como-pandemia
- Sreenath K, Batra P, Vinayaraj EV, Bhatia R, SaiKiran K, Singh V, et al . Coinfections with Other Respiratory Pathogens among Patients with COVID-19. Microbiol Spectr 2021; 9(1):e0016321. https://doi.org/10.1128/Spectrum.00163-21
- Parra-Lara LG, Martinez-Arboleda JJ, Rosso F. Azithromycin and SARS-CoV-2 infection: Where we are now and where we are going. J Glob Antimicrob Resist 2020;22:680-684. https://doi.org/10.1016/j.jgar.2020.06.016
- Heinige P, Slovakova L, Vo.kova J, Leova LN, Ta.kova A, Kripnerova K, et al . Impact of the COVID-19 Pandemic on Pediatric Pneumonia Outcomes: A Five- Year Retrospective Cohort Study. Infect Drug Resist 2025;18:3511-3525. https://doi.org/10.2147/IDR.S524238
- Ai L, Fang L, Zhou C, Liu B, Yang Q, Gong F. The impact of the COVID-19 pandemic on Staphylococcus aureus infections in pediatric patients admitted with community acquired pneumonia. Sci Rep 2024;14(1):15737. https://doi.org/10.1038/s41598-024-66071-4
- Sulayyim HJA, Ismail R, Hamid AA, Ghafar NA. Antibiotic Resistance during COVID-19: A Systematic Review. Int J Environ Res Public Health 2022;19(19):11931. https://doi.org/10.3390/ijerph191911931
- Tubaro C, Dominguez R, Hinojosa M, Mosca S, De Leo G, Cabrera, R. Prevalencia de Staphylococcus aureus y su sensibilidad antibio.tica en aislamientos en infecciones de piel y partes blandas en pacientes ambulatorios. Actual Sida Infectol 2024;32(114):9-15. https://doi.org/10.52226/revista.v32i114.186
- Worku M, Belay S, Molla T, Amare A, Tigabie M, Taher W et al . Bloodstream infections with emphasis on Methicillin-resistant Staphylococcus aureus at the University of Gondar Comprehensive Specialized and Referral Hospital, Northwest Ethiopia. BMC Infect Dis 2025;25(1):663. https://doi.org/10.1186/s12879-025-11074-3
- Ahmed OB, Bahwerth FS, Alsafi R, Elsebaei EA, Gamal T, Theyab A, et al . The Prevalence and Antimicrobial Susceptibility of Methicillin-Resistant Staphylococcus aureus Before and After the COVID-19 Pandemic in a Tertiary Saudi Hospital. Cureus 2024;16(2):e54809. https://doi.org/10.7759/cureus.54809
- Zhao Ch, Guo Z, Li X, Ji Y, Li T, Li M, et al . Effect of the COVID-19 epidemic on drug resistance of Staphylococcus aureus infection. J Microbiol Infect Dis 2024;14(1):13-20. https://doi.org/doi:10.5455/JMID.2024.v14.i1.3
- Gauto M, Hinojal F, Alonso L, Ibarra B, Tejada N, Arcidiacono D et al . Infeccion primaria de la sangre asociada a cateter central en unidades de cuidados intensivos de adultos durante la pandemia de COVID-19 en la Argentina. Rev Hosp Ital B Aires [Internet]. 2024;44(3):e0000375. https://doi.org/10.51987/rev.hosp.ital.b.aires.v44i3.37522
- Lopez-Jacome LE, Fernandez-Rodriguez D, Franco- Cendejas R, Camacho-Ortiz A, Morfin-Otero MDR, Rodriguez-Noriega E, et al . Increment Antimicrobial Resistance During the COVID-19 Pandemic: Results from the Invifar Network. Microb Drug Resist 2022;28(3):338-345. https://doi.org/10.1089/mdr.2021.0231
- Zarfel G, Schmidt J, Luxner J, Grisold AJ. No Changes in the Occurrence of Methicillin-Resistant Staphylococcus aureus (MRSA) in South-East Austria during the COVID-19 Pandemic. Pathogens 2023;12(11):1308. https://doi.org/10.3390/patogenos12111308
- Golli AL, Zlatian OM, Cara ML, Olteanu M. Pre- and Post-COVID-19 Antimicrobial Resistance Pattern of Pathogens in an Intensive Care Unit. Pharmaceuticals (Basel) 2024;17(4):407-415. https://doi.org/10.3390/ph17040407
