Introducción
Acinetobacter baumannii (A. baumannii) es un importante patógeno nosocomial que causa infecciones graves como neumonía asociada con ventilación mecánica, infección del torrente sanguíneo, infección del tracto urinario, meningitis e infecciones de heridas, particularmente en pacientes recluidos en unidades de cuidado intensivo (1, 2). Este microrganismo se ha convertido en un reto sanitario en todo el mundo debido a su resistencia a los antimicrobianos y su capacidad de diseminación (3). Además, la resistencia a la desecación permite al organismo sobrevivir en superficies inanimadas durante largos períodos de tiempo, lo que contribuye a su transmisión dentro del entorno hospitalario, lo que resulta en brotes y persistencia endémica (1). Su resistencia antimicrobiana intrínseca y adquirida es una grave amenaza para el éxito del tratamiento de las infecciones por A. baumannii (4). La resistencia creciente a los carbapenémicos, que se ha intensificado durante las últimas décadas, ha limitado de manera crítica el uso de estos antimicrobianos de primera línea para tratar infecciones causadas por este microorganismo (3). A. baumannii resistente a carbapenémicos ha sido clasificado como patógeno de prioridad 1 (“crítico”) en la lista de la Organización Mundial de la Salud para la investigación y el desarrollo de nuevos antibióticos (5), y los Centros para el Control y la Prevención de Enfermedades (CDC) lo han situado en la categoría de amenaza urgente para la salud pública. En 2017, se estimó que A. baumannii resistente a carbapenémicos ocasionó aproximadamente 8.500 infecciones en pacientes hospitalizados en los Estados Unidos, con unas 700 muertes asociadas, reflejando su alta carga clínica y epidemiológica (6).
La resistencia a los carbapenémicos está mediada principalmente por las betalactamasas de clase D hidrolizantes de carbapenémicos de tipo OXA adquiridas [oxacilininasas (OXAs)], codificadas por blaOXA-23-like , blaOXA-40-like , blaOXA-58-like , blaOXA-143- like y blaOXA-235-like (7-9). Con menos frecuencia, la resistencia a los carbapenémicos en A. baumannii está mediada por metalo-betalactamasas de clase B (MBL) como IMP, NDM, SIM y VIM (1, 10) y solo raramente por betalactamasas de clase A KPC y GES (11, 12). Por lo tanto, este estudio fue diseñado para evaluar la distribución de los genes (blaOXA23-like, blaOXA24- like, blaOXA58, blOXA143, blaKPC-like y blaVIM-like) involucrados en mecanismos de resistencia enzimático a carbapenémicos, en un grupo de aislados clínicos del Complejo Acinetobacter baumannii.
Materiales y métodos
Cepas bacterianas: En el presente estudio se analizaron 283 aislados clínicos de A. baumannii resistentes a carbapenémicos provenientes de tres centros hospitalario de la ciudad de Caracas: Hospital Dr. José María Vargas, Hospital Domingo Luciani y Centro Médico de Caracas. Los cuales fueron identificados como Complejo A. calcoaceticus-baumannii empleando el sistema automatizado de identificación microbiológica Microscand (Beckman Coulter, Inc.). La identificación definitiva de género y especie se llevó a cabo mediante análisis de la secuencia del gen rrs que codifica a la subunidad 16S del ARN ribosomal. La susceptibilidad antimicrobiana de estos aislados a los carbapenémicos evaluados (imipenem y meropenem) fue determinada empleado el método de difusión del disco y el nivel de resistencia por medio de las concentraciones inhibitorias mínimas (CIM) en agar (13).
Identificación molecular de genes de resistencia: Los aislados clínicos de A. baumannii en estudio fueron analizados para detectar la presencia de una serie de genes que codifican para las carbapenemasas tipo OXA (blaOXA23-like, blaOXA24-like, blaOXA58y blOXA143), serinoenzimas (blaKPC-like) y metalobetalactamasas (blaVIM-like). Los genes que codifican para las principales betalactamasas que hidrolizan carbapenémicos, fueron detectados por PCR amplificando la región codificante completa de cada gen y se usaron pares de iniciadores específicos (Tabla 1). Las bandas fueron detectadas por transiluminación con luz ultravioleta (FOTO/Prep) y documentada fotográficamente. Los productos de PCR, previamente purificados (QIAquick. - QIAGEN), fueron enviados a la unidad de estudios genéticos y forenses (UEGF) del Instituto Venezolano de Investigaciones Científicas (IVIC) para ser secuenciados. Posteriormente, las secuencias obtenidas fueron comparadas con aquellas disponibles en el GenBank (htpp://www.ncbi.nlm.nih. gov/BLAST), haciendo un BLAST para confirmar la presencia de dichos genes en las cepas A. baumannii analizadas.
Tabla 1.
Oligonucleótidos utilizados para la amplificación y secuenciación de los genes que codifican para las principales betalactamasas que hidrolizan carbapenémicos.

pb (pares de bases)
Fuente: Elaboración propia
Cepas controles
Como control de calidad para las reacciones de PCR se utilizaron, una cepa de K. pneumoniae productora de KPC cuya característica de carbapenemasa fue evaluada mediante detección fenotípica, y cedida por el laboratorio de Bacteriología del Hospital Dr. Domingo Luciani; una cepa de Pseudomonas aeruginosa productora de VIM proporcionada por el Instituto Nacional de Higiene Rafael Rangel, las cepas A. baumannii FER productora de OXA23, A. baumannii CLA productora de OXA 40, y A. baumannii BMBF98 productor de OXA143, adquiridas en el Servicio de Bacteriología - Virología - Higiene - Parasitología. Hospital Central Universitario de Bicetre-Francia.
Resultados
Del conjunto de genes que codifican para las carbapenemasas tipo OXA (blaOXA23-like, blaOXA24-like, blaOXA58y blOXA143), serinoenzimas (blaKPC-like) y metalo-betalactamasas (blaVIM-like), solo un grupo de ellos lograron ser amplificado a partir de los aislados. De los genes que codifican para las carbapenemasas tipo OXA, el uso de iniciadores específicos para los genes blaOXA23-like permitió la obtención de un amplicon de 1058 pb. Este producto de PCR fue secuenciado posteriormente y analizado mediante el programa BLAST, el cual reveló que la secuencia nucleotídica presentaba una 99% de similitud con la secuencia del gen blaOXA23 incluida en la base de datos del GenBanck. Dicho gen logró ser amplificado en 23 aislados (8,1%) de los A. baumannii evaluados en el presente estudio (Figura 1). Los iniciadores específicos para el gen blaOXA24-like permitió la obtención de un amplicon de1000 pb en 1 sola cepa (Figura 2). Una vez purificado el producto de la PCR, el mismo fue secuenciado y analizado mediante el programa BLAST. Este análisis evidenció que la secuencia nucleotidica tenía un 99% de similitud con la secuencia del gen blaOXA72 . De los aislados clínicos analizados, 28 cepas generaron un amplicón de 528 pb mediante PCR. La secuenciación de estos productos y su análisis por BLAST revelaron una similitud del 99% con la secuencia del gen blaOXA-58 (Figura 3). Asimismo, se evaluó la presencia del gen blaOXA-143 , para el cual la técnica de PCR produjo un amplicón de 825 pb, mostrando igualmente una similitud del 99% con la secuencia depositada en GenBank. Sin embargo, dicho gen no fue detectado en ninguna de las cepas incluidas en este estudio.
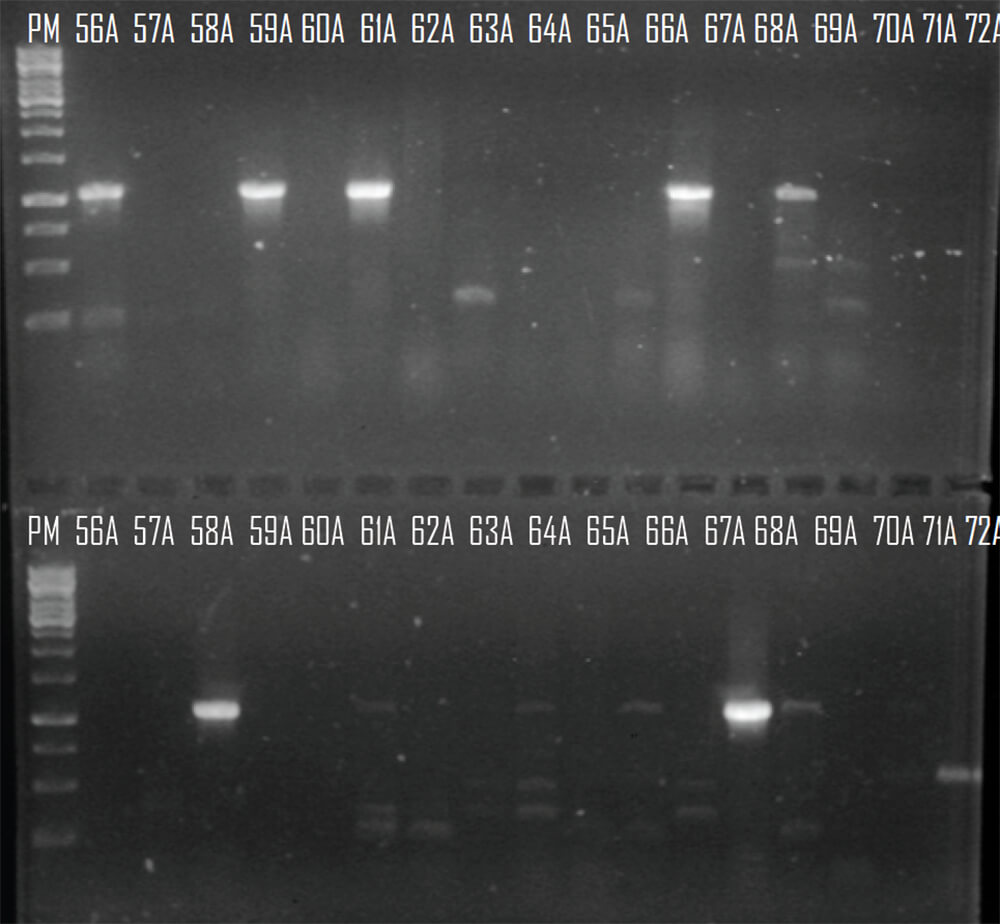
Figura 1. Registro fotográfico de un gel de agarosa al 0,8% donde se observan los amplificados del gen que codifica para la carbapenemasa OXA 23. Líneas 1 y 19: 1Kb DNA Ladder (BioLabs), Línea 2 y 3: Control positivo y negativo, Líneas 4-18 (41A-55A) y 20-36 (56A-72A) aislados clínicos provenientes del Hospital Dr. Domingo Luciani
Fuente: Elaboración propia.
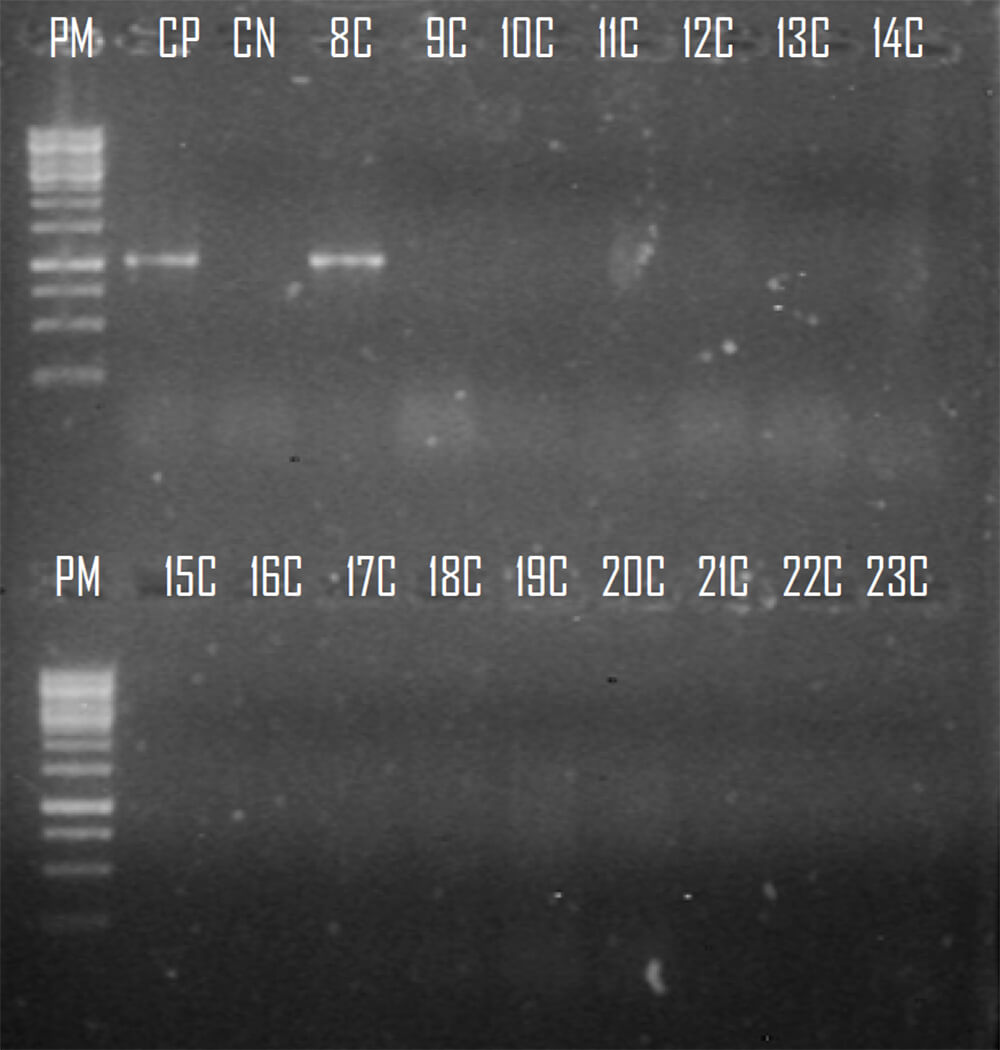
Figura 2. Amplificados del gen que codifica para la carbapenemasa OXA 72. Líneas 1 y 11: 1Kb DNA Ladder (BioLabs), Línea 2 y 3: Control positivo y negativo, Líneas 4-10 (8C-14C) y 12-20 (15C-23C) aislados clínicos provenientes del Centro Médico de Caracas.Fuente: Elaboración propia
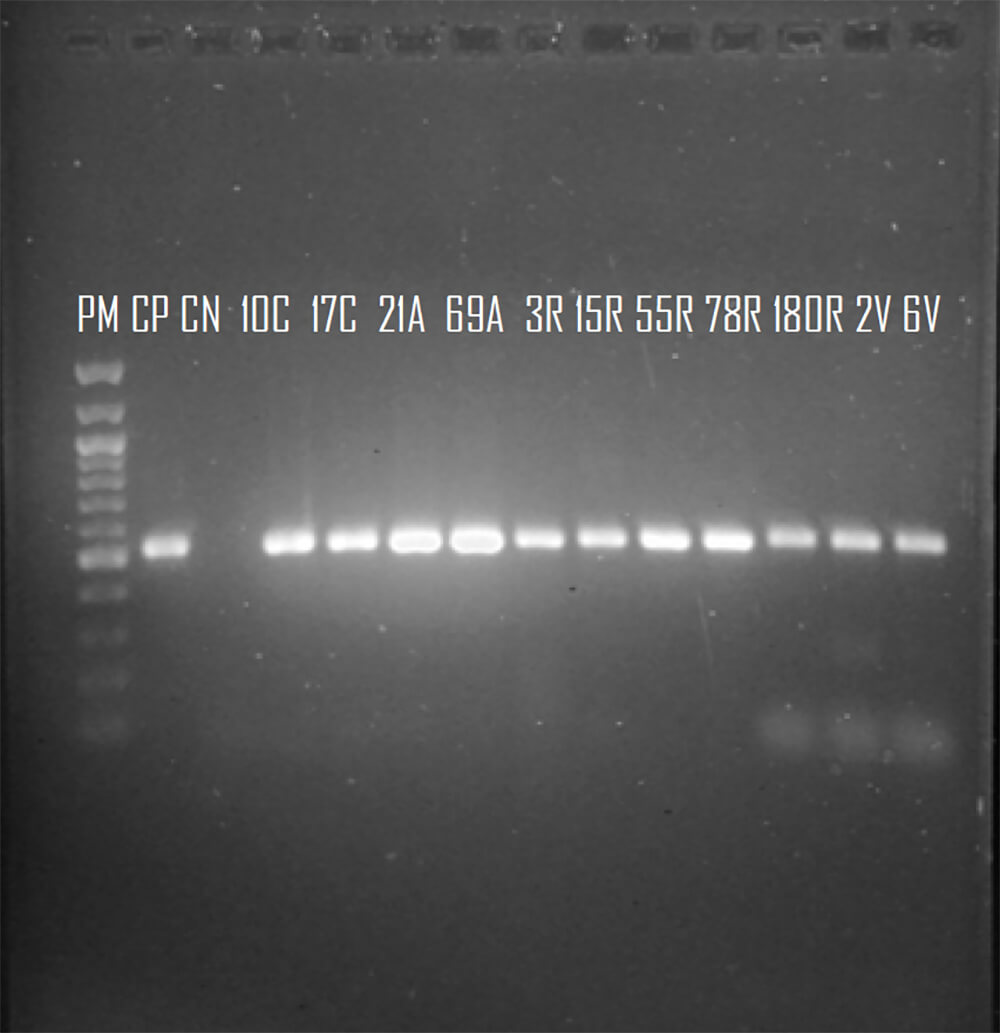
Figura 3.
Registro fotográfico de un gel de agarosa al 0,8% donde se observan los amplificados del gen que codifica para OXA 58. Línea 1: 100 pb DNA Ladder (BioLabs), Línea 2 y 3: Control positivo y negativo, Líneas 4-14 aislados clínicos provenientes del Centro Médico de Caracas, Hospital Dr. Domingo Luciani y Hospital Vargas.
Fuente: Elaboración propia
Mediante la técnica de la PCR y utilizando iniciadores específicos para amplificar los genes que codifican para metalo-betalactamasas, solo se logró obtener el amplificado correspondientes de las cepas control. Con los iniciadores para los genes blaVIM-like , se originó un producto de 780 pb, el cual al ser secuenciado el mismo tenían un 100% de similitud con secuencia correspondiente al gen blaVIM-2 almacenado en la base de datos del Genbanck. Sin embargo, no se logró detectar estos genes en los aislados clínicos de A. baumannii analizados. Empleando los iniciadores para los genes blaKPC-like se obtuvo un producto de PCR de 700 pb de la cepa control que al ser secuenciado el mismo presentó un 99% de similitud con la secuencia correspondiente al gen blaKPC-19 . Este gen tampoco logró ser amplificado en las 283 cepas evaluadas.
Discusión
La producción de OXA-23 es señalada como el mecanismo de resistencia a los carbapenémicos encontrados con mayor frecuencia en los hospitales de todo el mundo (17, 18). Pero en el presente estudio, el gen asociado con este mecanismo de resistencia solo fue detectado en el 8,1% (23/283). En un estudio previo, en Caracas-Venezuela, se logró detectar blaOXA- 23-like en el 93,4% de los aislados de A. baumannii (17). Desconociéndose los posibles factores que pudieran influir en los resultados discrepantes obtenidos con la presente investigación. Existen estudios conducidos en un mismo país donde previamente se asocia la resistencia a los carbapenémicos con la presencia de un determinado tipo de carbapenemasa y posteriormente se describe la prevalencia de otra enzima con actividad carbapenemasa asociada con la resistencia a estos antimicrobianos (19). El gen blaOXA-72 , logró ser amplificado en un solo aislado clínico de A. baumannii , constituyéndose este estudio el primer reporte de carbapenemasa tipo OXA-72 en Venezuela. La aparición de casos esporádicos con esta enzima, también ha sido reportados en Colombia y Estados Unidos (20, 21). Por el contrario, otros autores han reportado la diseminación de un clon endémico de A. baumannii productor de OXA-72, el cual fue el responsable de los brotes y de la alta frecuencia del gen blaOXA-72 (97%) que codifica para la carbapenemasa OXA-72 (19). El primer reporte de OXA-58 en Venezuela fue documentado por Salazar E. et al. (22), quienes lograron identificar la presencia de esta enzima en el 10% de los aislados clínicos de A. baumannii. Siendo estos resultados muy similares a los obtenidos en la presente investigación (9,9%). Por el contrario, en Bolivia se logró detectar blaOXA-58-like en el 39,4% de los aislados de A. baumannii (23). Y en Europa la enzima OXA-58 también ha sido identificada y considerada endémica en países como Francia, Turquía y Grecia (24). OXA- 143 fue descrita por primera vez en un aislado clínico de A. baumannii multirresistente en Brasil durante la realización de un estudio multicéntrico. Y luego se describió una elevada prevalencia de blaOXA-143 (58,3%) (25). Inicialmente OXA-143 se encontraba de forma exclusiva en Brasil, sin embargo, en Irán se describió que el 14,43 % de los aislados clínicos de A. baumannii resistentes a carbapenémicos fueron positivos para esta enzima (26). En cambio, en nuestro estudio no se logró detectar la presencia de blaOXA-143 . En Puerto Rico se logró identificar la presencia de la enzima KPC en el 3,4% de los Acinetobacter resistentes a carbapenémicos (12). No obstante, porcentajes más elevados (22,5%) han sido reportados en México (27). Por el contrario, en el presente estudio no se logró detectar la presencia de blaKPC-like . Un dato importante para considerar es que la cepa empleada como control positivo para la identificación del gen blaKPC provenía de un aislado clínico de K. pneumoniae y previamente se ha reportado, en un mismo hospital, que inicialmente la presencia de blaKPC-like fue identificada en especies de Klebsiella y posteriormente en A. baumannii. Sugiriendo la posible transmisión horizontal, debido a que esta carbapenemasa ha sido asociada con elementos genéticos móviles los cuales pueden ser transferidos de una bacteria a otra (27,28). Las enzimas VIM han sido identificadas muy raramente en A. baumannii, asimismo en algunas regiones del mundo solo pocos aislados son productores de metalobetalactamasas (29,30). En nuestro estudio no se logró detectar la presencia de blaVIM en ninguno de los aislados clínicos evaluados, de manera similar a los resultados reportados en Colombia (31). En Venezuela, se ha reportado la presencia VIM, pero en aislados de Pseudomonas aeruginosa y Klebsiella pneumoniae resistentes a carbapenémicos (32,33). Razón por lo cual es necesaria su detección continua, debido a la plasticidad genética de A. baumannii y el papel que juegan los elementos móviles en la trasmisión de la resistencia (28). La mayoría de los estudios publicados hasta la fecha hacen referencia a la adquisición de carbapenemasa tipo OXA como uno de los mecanismos predominantes para adquirir resistencia a los carbapenémicos en especies de Acinetobacter (17,18). Sin embargo, en la presente investigación se encontró un elevado porcentaje (81,6%) de aislados en las cuales no fue posible evidenciar la presencia de ninguno de los genes que codifican carbapenemasas. La disminución de la permeabilidad de la membrana externa pudiera estar jugando un papel importante en la resistencia a carbapenémicos (34), al igual que la sobreexpresión de las bombas de eflujo parece contribuir en el incremento de la Concentración Inhibitoria Mínima de meropenem (21). Por otro lado, la híperproducción de AmpC reduce significativamente la sensibilidad a cefalosporinas de cuarta generación y a los carbapenémicos, si se produce también la pérdida de alguna porina relacionada con la resistencia antimicrobiana o la expresión exagerada de bombas de flujo (35).
Finalmente, este trabajo representa un aporte importante a la epidemiología molecular de A. baumannii ya que en nuestro estudio se encontró que en un elevado número de aislados (231) resistentes a carbapenémicos, no fue posible evidenciar la presencia de ninguno de los genes que codifican carbapenemasas. Esto nos permiten pensar que, pudieran estar presentes otros mecanismos de resistencia a betalactámicos de naturaleza no enzimáticas que probablemente sean responsables de la resistencia a carbapenémicos o a la presencia de otras carbapenemasas no evaluadas en el presente estudio.
Conclusiones
Los genes blaOXA-23, blaOXA-72y blaOXA-58 fueron detectados en aislados resistentes a los carbapenémicos. Por el contrario, los genes blaOXA-143, blakpcy blaVIM no estuvieron presentes en ninguno de los aislados clínicos evaluados. En un elevado número de A. baumannii (81,6%) resistentes a los carbapenémicos no fue detectado ningunos de los genes que codificara las diversas carbapenemasa evaluadas. Es posible que la resistencia en estos aislados este mediada por la combinación de otros mecanismos enzimáticos y/o no enzimáticos los cuales no fueron ensayados en el presente estudio.
Referencias
- Peleg A, Seifert H, Paterson D. 2008. Acinetobacter baumannii: emergence of a successful pathogen. Clin Microbiol Rev 21(3):538-582. https://doi.org/10.1128/CMR.00058-07
- Villar M, Cano ME, Gato E, Garnacho-Montero J, Miguel Cisneros J, Ruíz de Alegría C, et al. Epidemiologic and clinical impact of Acinetobacter baumannii colonization and infection: a reappraisal. Medicine (Baltimore) 93(5):202-210. https://doi.org/10.1097/MD.0000000000000036
- Doi Y, Murray GL, Peleg AY. Acinetobacter baumannii: evolution of antimicrobial resistance-treatment options. Semin Respir Crit Care Med 2015;36(1):85-98. https://doi.org/10.1055/s-0034-1398388
- Abbott I, Cerqueira G, Bhuiyan S, Peleg A. Carbapenem resistance in Acinetobacter baumannii: laboratory challenges, mechanistic insights and therapeutic strategies. Expert Rev Anti Infect Ther 2013;11(4):395- 409. https://doi.org/10.1586/eri.13.21
- World Health Organization. Global priority list of antibiotic-resistant bacteria to guide research, discovery, and development of new antibiotics. Geneva: World Health Organization; 2024. https://www.cdc.gov/drugresistance/pdf/threats-report/2019-ar-threatsreport-508.pdf
- Higgins P, Poirel L, Lehmann M, Nordmann P, Seifert H. OXA-143, a novel carbapenem-hydrolyzing class D beta-lactamase in Acinetobacter baumannii. Antimicrob Agents Chemother 2009;53(12):5035-5038. https://doi.org/10.1128/AAC.00856-09
- Higgins P, Pérez-Llarena F, Zander E, Fernández A, Bou G, Seifert H. OXA-235, a novel class D β-lactamase involved in resistance to carbapenems in Acinetobacter baumannii. Antimicrob Agents Chemother 2013;57(5):2121-2126. https://doi.org/10.1128/AAC.02413-12
- Poirel L, Nordmann P. Carbapenem resistance in Acinetobacter baumannii: mechanisms and epidemiology. Clin Microbiol Infect 2006;12:826-836. https://doi.org/10.1111/j.1469-0691.2006.01456.x
- Poirel L, Bonnin R, Nordmann P. Genetic basis of antibiotic resistance in pathogenic Acinetobacter species. IUBMB Life 2011;63(12):1061-1067. https://doi.org/10.1002/iub.532
- Moubareck C, Brémont S, Conroy M, Courvalin P, Lambert T. GES-11, a novel Integron-associated GES variant in Acinetobacter baumannii. Antimicrob Agents Chemother 2009;53(8):3579-3581. https://doi.org/10.1128/AAC.00072-09
- Robledo I, Aquino E, Santé M, Santana J, Otero D, León C, and Vásquez G. Detection of KPC in Acinetobacter spp. In Puerto Rico. Antimicrob. Agents. Chemother. 2010;54(3):1354-1357. https://doi.org/10.1128/AAC.00899-09
- González G, Howard T. Epidemiología molecular y convencional de aislados clínicos de Acinetobacter baumannii resistentes a carbapenémicos. Rev Fac Med 2025;48(1):4-30. [cited 10 Sep. 2025]. Disponible en: https://saber.ucv.ve/ojs/index.php/rev_fmed/article/view/30317
- Wolter D, Khalaf N, Robledo I, Vázquez G, Santé M, Aquino E, et al. Surveillance of carbapenem-resistant Pseudomonas aeruginosa isolates from Puerto Rico medical center hospitals: Dissemination of KPC and IMP-18 β-lactamases. Antimicrob Agents Chemother 2009;53(4):1660-1664. https://doi.org/10.1128/AAC.01172-08
- Jeon C, Jeong S, Bae I, Kwon S, Lee K, Young D, et al. Investigation of a nosocomial outbreak of imipenemresistant Acinetobacter baumannii producing the OXA-23 ß-lactamase in Korea. J Clin Microbiol 2005;43(5):2241-2245. https://doi.org/10.1128/JCM.43.5.2241-2245.2005
- Héritier C, Poirel L, Lambert T, and Nordmann P. Contribution of acquired carbapenem-hydrolyzing oxacillinases to carbapenem resistance in Acinetobacter baumannii. Antimicrob. Agents Chemother 2005;49(8):3198-3202. https://doi.org/10.1128/AAC.49.8.3198-3202.2005
- Cuaical N, Delgado Y, Anzola Y, Marcano D. Torres L. Detección de carbapenemasa tipo OXA en aislados de Acinetobacter baumannii de diferentes centros hospitalarios de Caracas, Venezuela. Rev Soc Ven Microbio 2012;32(12):95-100. https://doi.org/
- Rodríguez C, Nastro M, Flores S, Rodriguez M, Spinozzi M, Bruni G, et al. Epidemiología molecular de aislados de Acinetobacter baumannii resistentes a carbapenems en Argentina. Rev Argent Microbiol 2019;51(3):247- 250. https://doi.org/10.1016/j.ram.2017.12.004
- Franolic-Kukina, I, Bedenic B, Budimir A, Herljevic Z, Vranes J, Higgins P. Clonal spread of carbapenemresistant OXA-72-positive Acinetobacter baumannii in a Croatian university hospital. Int J Infect Dis 2011;15(10):706-709. https://doi.org/10.1016/j.ijid.2011.05.016
- Tian G, Adams-Haduch J, Bogdanovich T, Pasculle A, Quinn J, Wang H, et al. Identification of Diverse OXA-40 Group Carbapenemases, Including a Novel Variant, OXA-160, from Acinetobacter baumannii in Pennsylvania. Antimicrob. Agents Chemother. 2011;55(1):429-432. https://doi.org/10.1128/AAC.01155-10
- Saavedra S, Cayo R, Gales C, Leal A, Saavedra C. Early dissemination of OXA-72 producing Acinetobacter baumannii strain in Colombia: a case report. Braz J Infect Dis 2014;18(6):678-680. http://dx.doi.org/10.1016/j.bjid.2014.05.017
- Salazar de Vegas E, Nieves B, Araque M, Velasco E, Ruiz J, Vila J. Outbreak caused by Acinetobacter strain RUH 1139 in an Intensive Care Unit. Infect. Conrol. Hosp. Epidemiol. 2006;27(4):397-403. https://doi.org/10.1086/503177.
- Fernández E, Bustamante Z, Zamora J, Zabalaga S, Pinto J, Funes F, et al. Determinación de Carbapenemasa y su relación con estructuras genéticas en aislamientos clínicos de Acinetobacter baumannii de hospitales de la ciudad de Cochabamna. BIOFARBO. 2009;17(1):30-38.
- Poirel L, Lebessi E, Heritier C, Patsoura A, Foustoukou M, Nordmann P. Nosocomial spread of OXA-58-positive carbapenem-resistant Acinetobacter baumannii isolates in a paediatric hospital in Greece. Clin Microbiol Infec 2006;12(11):1138-1144. https://doi.org/10.1111/j.1469-0691.2006.01537.x
- Antonio C, Neves R, Medeiros M, Mamizuka E, Elmor de Araujo M, Lincopan N. High prevalence of carbapenemresistant Acinetobacter baumannii carrying the bla OXA-143 gene in Brazilian hospitals. Antimicrob Agents Chemother 2011;55(3):1322-1323. https://doi.org/10.1128/AAC.01102-10
- Sarikhani Z, Nazari R, Nateghi M. First report of OXA-143-lactamase producing Acinetobacter baumannii in Qom, Iran. Iran J Basic Med Sci 2017;20(11):1282-1286. https://doi.org/10.22038/IJBMS.2017.9490
- Rodríguez M, López S, Reyes J, Vélez F, Ochoa L, Fernández L, et al. Emerging in Mexico of carbapenem resistance KPC-carrying Acinetobacter baumannii. Annual Meeting IDSA. Boston. 2011;397.
- Curiao T, Morosini M, Ruiz-Garbajosa P, Robustillo A, Baquero F, Coque TM, et al. Emergence of bla KPC- 3-Tn4401a associated with a pKPN3/4-like plasmid within ST384 and ST388 Klebsiella pneumoniae clones in Spain. J Antimicrob Chemotherapy 2010;65(8):1608-1614. https://doi.org/10.1093/jac/dkq174
- Cornaglia G, Giamarellou H, Rossolini G. Metallo-β- lactamases: a last frontier for β-lactams? Lancet Infect Dis 2011;11(5):381-393. https://doi.org/10.1016/S1473-3099(11)70056-1
- MinionPro-Regular;MinionPro-It; Amudhan MS, Sekar U, Kamalanathan A, Balaraman S. blaIMP and blaVIM mediated carbapenem resistance in Pseudomonas and Acinetobacter species in India. J Infect Dev Ctries 2012;6(11):757-762. https://doi.org/10.3855/jidc.2268
- Orquidea J, Mantilla J, Valenzuela E, Fernandez F, Alvarez C, Osorio E. Molecular characterization of Acinetobacter baumannii isolations from a burns unit in a third level attention hospital in Bogota. Infectio 2006;10(2):71-78. [cited 10 Sep. 2025]. Disponible en: https://revistainfectio.org/P_OJS/index.php/infectio/article/view/171/213
- Sanchez D, Marcano D, Spadola E, Leon L, Payares D, Ugarte C, et al. Metaloenzimas tipo VIM detectadas en aislamientos clinicos en Pseudomonas aeruginosa en cuatro hospitales en Venezuela. INHRR. 2008;39(2):17- 22. [cited 10 Sep. 2025]. Disponible en: https:// ve.scielo.org/scielo.php?script=sci_arttext&pid=S0798-04772008000200004
- Marcano D, Pasteran F, Rapoport M, Faccone D, Ugarte C, Salgado N, et al . First isolation of a VIM-producing Klebsiella pneumoniae from a seven-year-old child in Venezuela. J Infect Dev Ctries 2008;2(3):241-244. https://doi.org/10.3855/jidc.270
- Takagi E, Lincopan N, Cassettari V, Passadore L, Mamizuka E, Martinez M. Carbapenem-Resistan Acinetobacter baumannii outbreak at University Hospital. Braz J Microbiol 2009;40(2):339-341. https://doi.org/10.1590/S1517-838220090002000024
- Navarro F, Calvo J, Canton R, Fernandez-Cuenca F, Mirelis B. Deteccion fenotipica de mecanismos de resistencia en microorganismos gramnegativos. Enferm Infecc Microbiol Clin 2011;29(7):524-534. https://doi.org/10.1016/j.eimc.2011.03.011
